Thérapeutique
Publié le 21 avr 2009Lecture 10 min
Les nouvelles molécules par voie orale vont-elles (enfin) faire progresser l'anticoagulation chronique ?
L. DROUET, Angio-hématologie, Hôpital Lariboisière, Paris
Les anticoagulants oraux n’existent aujourd’hui que sous une seule forme, les AVK. Quels que soient nos efforts pour les manier le mieux possible, ce maniement est encore imparfait pour ne pas dire pire. En effet, il n’est que partiellement efficace ; il est particulièrement dangereux et contraignant pour les patients quelles que soient les aides qu’on essaie de leur proposer (allégement des contraintes alimentaires, automesures, etc.). Il y a cinq ans une énorme attente accompagnait la mise sur le marché du mélagatran. Malheureusement, une toxicité hépatique, bien que d’incidence exceptionnelle, est venue gâcher la fête. C’est dire tout l’enjeu de la mise sur le marché de nouveaux anticoagulants oraux qui pourraient révolutionner la prise en charge des pathologies thromboemboliques.
Le principal atout des nouveaux anticoagulants est leur voie d’administration orale. En termes d’efficacité comparativement aux thérapeutiques actuelles, on ne connaît que l’efficacité en prévention de la maladie thromboembolique veineuse (MTEV) en chirurgie orthopédique majeure (prothèses totales de hanche et de genou, PTH et PTG). Il apparaît dans les études de phase III que leur profil de tolérance est satisfaisant. On peut donc espérer que la thromboprophylaxie par les nouveaux anticoagulants oraux ouvre une nouvelle ère dans la prise en charge de la MTEV.
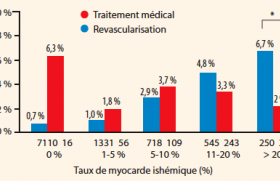
Le premier à être commercialisé est une antithrombine directe, le dabigatran etexilate ou Pradaxa®. Étant donné les avatars de son prédécesseur, le mélagatran (Exanta®), cette molécule a et sera regardée à la loupe, tant bien sûr pour son efficacité que pour sa sécurité ; en dehors de la sécurité, évidente, en termes de risque hémorragique, nous serons aussi particulièrement attentifs à la toxicité hépatique et à un autre effet secondaire qui avait été moins médiatisé que l’effet hépatique mais n’en était pas moins préoccupant, l’augmentation de l’incidence d’événements coronariens aigus en particulier d’infarctus du myocarde chez les patients, même en prévention ou en traitement d’événement thromboembolique veineux.
Que savons-nous du dabigatran etexilate ou Pradaxa® ?
Une antithrombine directe
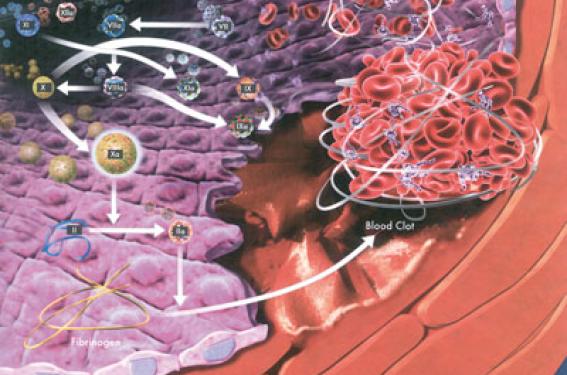
C’est une antithrombine directe existant uniquement sous forme orale (contrairement à son prédécesseur qui présentait une forme injectable pour le périopératoire) mais la pharmacocinétique de dabigatran etexilate ou Pradaxa® a permis de se passer de cette forme injectable pour ne permettre un traitement qu’oral. En tant qu’antithrombine directe, il va directement inhiber la thrombine circulante mais aussi la thrombine liée aux réseaux de fibrine des thrombi. Cet effet est plus difficilement obtenu avec les héparines qui agissent en complexe avec l’antithrombine, donc forment des molécules dont la grande taille ne leur permet pas de pénétrer au cœur des caillots. Le dabigatran etexilate ou Pradaxa® est spécifique de la thrombine (il n’inhibe pas d’autres sérines protéases).
Dans sa première utilisation thérapeutique testée, le dabigatran etexilate ou Pradaxa® est efficace dans la prévention des TVP en postopératoire précoce des prothèses totales de hanche et du genou, ce qui lui a valu sa première AMM.
Une pharmacologie assez particulière
Après administration orale, le dabigatran etexilate est rapidement transformé en sa forme active, le dabigatran. Le pic de concentration est atteint en 2 heures après l’absorption orale, mais 6 heures après la première prise le jour de l’intervention du fait des petits troubles du transit et de l’absorption en postopératoire immédiate et postanesthésie. Sa demi-vie est de 14-17 heures en postopératoire chez le sujet sain à fonction rénale normale ; son élimination est à 85 % rénale. Sa biodisponibilité à 6,5 % peut apparaître faible mais il existe peu de variabilité intra-individuelle et pas d’interaction avec l’alimentation. Sa pharmacocinétique suggère qu’il peut être administré en une seule fois pas jour ; d’ailleurs, les premières études de doses ont montré l’équivalence en termes d’efficacité de l’administration en une ou deux fois par jour. Il a donc été initialement développé en une seule prise quotidienne en prévention de la thrombose veineuse après chirurgie orthopédique de hanche et de genou. Après validation de ces études de phase III, il a obtenu l’AMM européenne en mars 2008 dans ces indications.
Une efficacité prouvée
L’étude de recherche de dose de phase II, a montré une diminution significative des TVP, dose-dépendante du dabigatran, mais associée à une augmentation des hémorragies majeures, aussi dose-dépendante. C’est pourquoi, il a été administré à demi-dose le jour de la chirurgie dans les phases III afin de diminuer le risque de saignement du site opératoire.
De plus, les études de phase III ont étudié, de manière intelligente, deux doses différentes de dabigatran etexilate ou Pradaxa® (150 mg ou 220 mg/j en une seule prise) et ont été comparées à l’énoxaparine. Ces études sur la thrombo-prophylaxie après PTG pendant 14 jours et PTH pendant un mois réalisées en Europe permettent de mettre en évidence :
• une non-infériorité en termes d’efficacité sur tous les événements thromboemboliques (totaux et majeurs) en comparaison avec l’énoxaparine après chirurgie prothétique de la hanche et du genou évaluée de manière séparée et distincte par des essais spécifiques ;
• une tolérance équivalente en termes de sécurité, qu’il s’agisse :
– d’hémorragies jugées sur tous les types de saignements (mineurs, majeurs), les pertes sanguines et les besoins transfusionnels ;
– de la toxicité hépatique jugée sur l’élévation des enzymes hépatiques et de la bilirubine ;
– de l’incidence de survenue d’accidents coronariens.
Pour diminuer le risque hémorragique, seule une demi-dose est administrée le premier jour entre 1 et 4 h (médiane = 3 h 30) après l’intervention.
Cependant, en comparaison avec le schéma américain (30 mg x 2 /j d’énoxaparine), il existe une non-infériorité seulement pour les événements thromboemboliques veineux majeurs (proximales, EP, décès).
Pas de surveillance biologique
La prédictibilité et la reproductibilité de sa pharmacocinétique confèrent au dabigatran le grand avantage de pouvoir être administré par voie orale, sans qu’une surveillance biologique ne soit nécessaire.
Il n’empêche que dans certaines conditions (patients en conditions extrêmes, doute sur une prise simple ou multiple, saignement pour lequel on a besoin de savoir si il est dû à un surdosage, nécessité d’un geste invasif d’urgence, etc.), on aimerait pouvoir posséder un test simple, disponible dans tous ou une grande majorité de laboratoires d’analyses médicales, qui précise si le niveau de taux plasmatique de dabigatran du patient se trouve dans la zone d’efficacité anticoagulante que l’on attendrait compte tenu de l’horaire de prélèvement par rapport à l’horaire d’administration. Le choix de ce test n’est pas encore établi mais le laboratoire producteur s’est engagée à le faire très prochainement.
Même avec monitoring, le dabigatran doit rester contre-indiqué chez les insuffisants hépatiques, les insuffisants rénaux sévères (clairance < 30 ml/min) et chez les femmes enceintes ou en âge de procréer sans contraception efficace. En effet, ces patients ont été exclus des études.
Une dose spécifique chez les sujets fragiles
Pour l’AMM Européenne en prévention des événements thromboemboliques veineux après PTH et PTG en 2008, il a été pris en compte qu’à la plus faible dose testée (150 mg/j), les sujets fragiles, c’est-à-dire âgés de plus de 75 ans ou porteurs d’une insuffisance rénale modérée, tirent le même bénéfice préventif des événements thromboemboliques veineux qu’avec la dose plus forte de 220 mg/j, au prix d’une incidence plus faible d’événements hémorragiques. Dans ces conditions, la dose de 150 mg/j est celle préconisée chez ces patients fragiles comme chez les patients recevant un traitement par amiodarone (en raison d’un risque d’interférence médicamenteuse).
C’est la première fois qu’une AMM est donnée avec une plus faible dose adaptée à ces sujets fragiles, évaluée tant en efficacité qu’en sécurité au cours des études pivots permettant enfin de privilégier la sécurité en améliorant, on l’espère, la tolérance de ce produit. Ceci est d’autant plus intéressant que la population est de plus en plus âgée en chirurgie orthopédique.
Jusqu’à présent, il n’existait aucun anticoagulant ayant une AMM spécifique chez les sujets > 75 ans, donc fragiles.
En pratique
Avec dabigatran etexilate ou Pradaxa® nous disposons d’une prévention orale, dès la première administration, du risque thromboembolique veineux après chirurgie orthopédique majeure. C’est une activité qui, traditionnellement, du moins à la phase initiale, était le domaine incontesté de la prévention par voie injectable. Il va falloir désacraliser le dogme selon lequel l’efficacité ne peut venir que de l’injectable : la voie orale est beaucoup plus facile, nécessite un temps infirmier moindre et procure au patient un confort indéniable. Mais il ne faut pas tomber dans la banalisation. Il va falloir changer les habitudes pour faire comprendre que ces deux gélules en une prise chaque jour sont aussi efficaces qu’une injection et aussi nécessaires que l’injection. Il faut donc y apporter la même attention pour que l’observance soit parfaite.
Ce nouveau traitement facilitera les traitements de durée moyenne (2 à 5 semaines) pour la prévention thromboembolique veineuse en fonction des types de chirurgie orthopédique majeure mais on attend encore plus de la suite du développement dans les autres indications de l’anticoagulation en chronique, à savoir le traitement curatif et la prévention secondaire de la maladie thromboembolique veineuse, dans la prévention des événements thromboemboliques artériels, en particulier des AVC chez les patients ayant une FA non valvulaire et, enfin, dans le syndrome coronaire aigu.
Que savons-nous du rivaroxaban ou Xarelto® ?
Peu de temps après le dabigatran apparaît le rivaroxaban, qui est d’une classe et d’un mode d’action différents. C’est le premier anticoagulant inhibiteur direct du facteur Xa, administré par voie orale, à être enregistré (AMM). Comme tous les premiers de la classe, il est intéressant de l’évaluer, et pour lui-même et pour la classe. Le ciblage du facteur Xa, facteur clef de la cascade de la coagulation, porte le bénéfice et le risque théorique d’avoir une efficacité antithrombotique et un risque hémorragique potentiels, tous deux dose-dépendants.
Le rivaroxaban a, comme tous les nouveaux antithrombotiques, été initialement développé dans la prévention des événements thromboemboliques veineux après chirurgie orthopédique majeure, ce qui a permis au rivaroxaban d’obtenir sa première AMM dans cette indication et d’être commercialisée sous le nom de Xarelto®.
Particularités pharmacologiques
Différents points méritent d’être soulignés d’un point de vue pharmacologique :
- une biodisponibilité d’environ 80-100 % ;
- une concentration maximale obtenue en 2 à 4 heures ;
- une demi-vie d’élimination terminale de 7 à 11 heures ;
- expliquant la fréquence d’une administration quotidienne ;
- la première administration à réaliser entre 6 et 10 heures après la fin de l’intervention s’explique par la précocité du pic plasmatique, une élimination rénale directe sous forme active pour un tiers et métabolisation hépatique par la voie des cytochromes P450 (3A4) pour deux tiers.
Les principales sources de variabilité sont la fonction rénale, la fonction hépatique et les inducteurs et inhibiteurs puissants du CYP450 3A4.
À quelle dose ?
La dose préconisée de 10 mg par jour correspond à celle déterminée par la recherche de dose (dose minimale donnant une efficacité en plateau pour les doses supérieures) et dose associée à l’incidence la plus basse des saignements.
Le nombre limité de précautions, de restrictions d’emploi et l’absence de contraintes d’adaptation posologique chez les sujets particuliers (âge, poids) sont expliqués par l’élimination à la fois par catabolisme hépatique, et rénale.
Une efficacité constante
Le rivaroxaban a montré une efficacité supérieure à la molécule de référence (énoxaparine) de niveau similaire pour toutes les différentes localisations et tous les types d’événements thromboemboliques veineux (qu’ils soient homo- ou controlatéraux à la chirurgie, distaux ou proximaux, compliqués d’embolie pulmonaire ou non, symptomatiques ou non, après chirurgie de hanche ou après chirurgie de genou).
Cette constance dans le degré de supériorité est expliquée par la cible anti-Xa de la molécule, qui est aussi la cible principale des HBPM, et d’autant qu’elles sont de plus bas poids moléculaire (leur forme extrême étant les pentasaccharides dont seul le fondaparinux est actuellement commercialisé).
Sécurité d’emploi
Les événements hémorragiques dans les études de recherche de dose montrent un effet dose-dépendant, ce qui explique la dose préconisée de 10 mg et les précautions d’emploi. Les événements hémorragiques dans les études de phase III avec le dabigatran et avec le rivaroxaban n’ont pas été quantifiées avec les mêmes critères ; les deux molécules ne sont donc pas directement comparables.
La durée d’indication après chirurgie orthopédique majeure est similaire pour les deux molécules et conforme aux recommandations de la SFAR : 2 semaines après PTG sauf s’il y a une indication à poursuivre plus longtemps, 4 à 5 semaines après PTH.
Bien que le dabigatran soit apparu avec une posologie adaptée pour les patients fragiles, il faut continuer à progresser dans la prise en charge des insuffisants rénaux, des obèses, des sujets très âgés chez lesquels les données sont peu nombreuses alors que ces patients sont de plus en plus nombreux et présentent les risques thrombotiques et hémorragiques les plus importants.
Quelle surveillance ?
Les difficultés de monitoring et d’adaptation de doses, bien connues avec les AVK, conduisent au développement des nouvelles classes de remplacement en essayant de n’avoir besoin d’aucun contrôle ni adaptation posologique. Pourtant, dans certaines conditions il y a nécessité de connaître le degré exact d’anticoagulation d’un patient. Pour les anti-Xa directs tels le rivaroxaban, le temps de Quick, le test de grande routine est sensible et donne une réponse d’allongement proportionnel à la concentration plasmatique dans une large gamme de concentrations. Ce test sera donc potentiellement utilisable à condition d’une indispensable normalisation.
En pratique
Ces molécules anticoagulantes actives par voie orale sont bien entendu en cours de développement dans la prévention des événements thromboemboliques artériels sur la fibrillation atriale, et dans la prévention d’extension et de récidive des événements thromboemboliques veineux, indication où les antivitamines K (AVK) sont le traitement de référence. Espérons que nous sommes à l’aube de voir disparaître les AVK de notre panoplie thérapeutique.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :