Lu pour vous
Publié le 15 déc 2021Lecture 8 min
Un patient, des complications
Jimmy DAVAINE, CHU Pitié-Salpêtrière, Paris
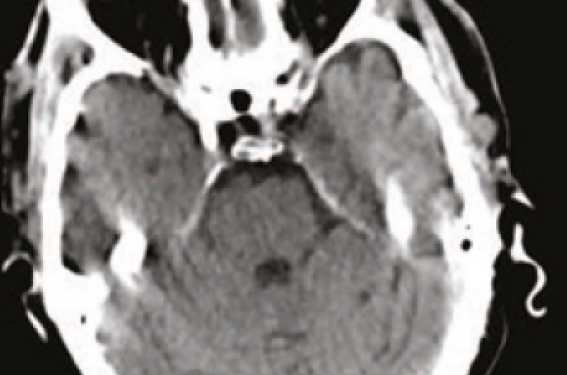
Un AAA avec sténoses des artères rénales, traité par endoprothèse. Les suites montrent des emboles multiples : blue toe syndrome, infarctus rénaux, AVC postérieur. Que dit la littérature sur tout cela.
Sténose des artères rénales : où en est-on ?
Le diagnostic et le traitement des sténoses de l’artère rénale (SAR) est complexe et sujet à controverse. La comorbidité la plus fréquemment associée est l’insuffisance cardiaque gauche : 54 % des patients porteurs d’insuffisance cardiaque gauche systolique présenterait une SAR, ce chiffre allant jusqu’à 68 % en cas d’insuffisance rénale associée. Le risque de la SAR est la mortalité plus que dialyse (44 % vs 16 % sur une médiane de 4 ans). La mortalité de l’insuffisance rénale chronique est augmentée d’un rapport de 1,5 lorsque la cause en est une SAR. Lorsque la SAR est significative (> 70-80 %), il y a une activation compensatrice du SRAA entraînant à son tour augmentation de l’activité du système sympathique, vasoconstriction, rétention sodée, activité inflammatoire. Ces mécanismes visent à augmenter la pression artérielle et sont réversibles au début par la levée de la sténose. Le contrôle de la PA va entretenir l’hypodébit rénal. À terme il se produit une fibrose néphronique avec dégradation de la fonction rénale.
Les présentations cliniques devant amener au dépistage des SAR sont les suivantes : HTA réfractaire, insuffisance rénale, dégradation de la fonction rénale (> 50 % en moins d’1 semaine), en particulier sous IEC/ARA2, OAP flash, décompensation cardiaque et asymétrie rénale > 1,5 cm.
L’écho-Doppler permet de faire le diagnostic en recherchant un ratio de PVS Ao/AR ≥ 3,5. Un index de résistance < 0,7 est prédictif d’un bon résultat de la revascularisation sur l’HTA. Le scanner permet de repérer les artères rénales accessoires et est possible jusqu’à un DFG de 30 ml/min. L’IRM a une bonne sensibilité et spécificité et les nouveaux agents de contraste au gadolinium sont moins néphrotoxiques qu’auparavant.
Le traitement médical est basé sur le contrôle de la tension artérielle par les IEC et ARA2 en priorité (la dégradation de la fonction rénale après leur instauration est en réalité assez rare et le traitement de la sténose fait rentrer les choses dans l’ordre). Le reste du traitement de la maladie athéromateuse est de rigueur. L’avènement des techniques endovasculaires a fait augmenter significativement le nombre de procédures. Les progrès médicamenteux ont été faits en parallèle rendant les « bonnes » indications difficiles à cerner (tableau).
Il faut comprendre la littérature
Il y a 3 essais randomisés contrôlés comparant traitement médical optimal (TMO) versus TMO + revascularisation : STAR (2009), ASTRAL (2009) et CORAL (2014). Les lésions inclues étaient des SAR > 50-60 %. Les études n’ont pas montré de bénéfices en termes d’amélioration de la fonction rénale et d’amélioration de tension artérielle. On voit que les sténoses étaient modérées et les patients les plus à même de bénéficier d’une procédure n’étaient pas inclus. L’insuffisance cardiaque était même un critère d’exclusion, c’est-à-dire que ces patients avaient une revascularisation mais n’étaient pas inclus !
Des séries non comparatives montrent un bon résultat de l’angioplastie mais apportent un niveau de preuve scientifiquement faible. On note que la revascularisation chirurgicale apporte un bénéfice par rapport à l’endovasculaire (métaanalyse de 47 articles 2009, Eur J Vasc Endovasc Surg 2009 ; 38 : 666-75) mais au prix d’une morbimortalité supérieure faisant réserver cette technique aux anatomies complexes (coral reef aorta) ou en cas d’anévrisme aortique associé ou de resténoses.
Hicks CW et al. Am J Kidney Dis 2021; doi.org/10.1053/j.ajkd.2021.06.025
Complications emboliques
Après mise en place d’une endoprothèse aortique (EVAR), 3-10 % des patients développent des complications ischémiques dont des ischémies digestives ou pelviennes et des membres inférieurs. Les emboles de cristaux de cholestérol représentent une complication grave avec un risque de morbimortalité élevée. Cette étude rétrospective se focalise sur les complications emboliques après EVAR. L’étude a porté sur 438 cas d’EVAR réalisés entre 2006-2009 (Zénith®, Cook [n = 205] pour les collets droits et larges et Excluder® Gore [n = 233] pour les collets proximaux et iliaques angulés ou petits diamètres). L’âge moyen des patients était de 76 ans et le suivi moyen était de 13,8 mois. Les complications emboliques étaient définies comme les ischémies digestives, les AVC et les événements athéroemboliques des membres inférieurs survenant dans les 7 jours suivant la chirurgie.
Résultats
Au total 438 patients avaient été inclus dans l’étude. Le succès technique était de 91 %. Les procédures associées à l’EVAR étaient les suivantes : TEVAR (11, 2,5 %), stent rénal (27, 6,2 %), stent iliaque (27, 6,2 %), embolisation hypogastrique (136, 31 %). On ne constatait pas de décès péri-opératoire. Neuf complications emboliques étaient recensées : 4 ischémies digestives traitées médicalement, 3 blue toe syndromes nécessitant des amputations d’orteils, 2 emboles de cristaux de cholestérol (décès par défaillance multiviscérale), 1 AVC. La survie à 1 an dans le groupe sans embole était de 97 % contre 86 % dans le groupe avec embole (p = 0,0003). Les facteurs identifiés comme prédictifs d’emboles étaient : tabagisme actif, insuffisance rénale préopératoire, présence d’une shaggy aorta (p < 0,0001). L’embolisation hypogastrique n’était pas prédictive d’événement embolique. À noter, la fréquence étaient de 3,4 % pour le Zénith® et de 0,9 % pour Excluder®.
Cette étude valide le fait que les complications emboliques, bien que rares (environ 2 %), sont graves. L’arrêt du tabac, le choix du matériel (et les statines à hautes dose ?) pourraient être bénéfiques dans les situations à risque.
Toya N et al. Surg Today 2014 ; 44 : 1893-9.
Le traitement des sténoses dysplasiques
La dysplasie fibromusculaire (DFM) est la 2e cause de sténose de l’artère rénale (SAR). Il se produit une prolifération anormale des cellules et une désorganisation de l’architecture de la paroi artérielle. Elle touche plutôt les femmes de 20-85 ans et provoque de l’HTA plus que de la perte néphronique. La revascularisation par angioplastie en est le traitement privilégié à l’heure actuelle.
Cette métaanalyse de la littérature a utilisé la méthodologie PRISMA. Sur 1 086 études, 36 ont été retenues pour analyse et 1 191 patients ont été traités par technique endovasculaire (moy : 27 patients par étude). La ponction fémorale était la règle, utilisation d’introducteurs de 5-7 F, rarement 8 F. Le succès technique était de 94 %. L’utilisation d’un stent était rapportée dans 7 études (20 patients au total). Les complications de la procédure se retrouvaient au niveau de l’abord (4,4 %) ou au niveau du rein (7 %) sous forme de dissection ou rupture-perforation d’artères rénales. Le taux global d’amélioration de la tension artérielle à 1 an, 3 ans et 5 ans était de 83 %, 74 % et 63 %. Le taux global de traitement complet de l’HTA était de 37 %. Il y avait de l’hétérogénéité entre les études notamment en ce qui concerne les définitions de l’amélioration de la tension artérielle.
L’efficacité du traitement par angioplastie était inversement corrélée à l’âge (p = 0,019) et à la durée (> 5 ans) d’évolution de l’HTA (p = 0,001). En moyenne, l’angioplastie permettait une diminution des chiffres de PAS de 35 mmHg et de PAD de 23 mmHg et en moyenne une réduction du nombre d’antihypertenseurs de 0,7. Il n’y avait pas d’amélioration de la fonction rénale. Enfin, les taux d’indemnité de resténose à 1 an, 3 ans et 5 ans étaient de 87 %, 73 % et 71 %.
Cette étude, malgré ses limitations (longue période, hétérogénéité entre les études, absence de groupe contrôle), a l’intérêt de se focaliser uniquement sur les SAR par DFM. Elle confirme les bénéfices de l’angioplastie (amélioration dans > 80 % des cas), surtout chez les patients les plus jeunes et traités précocement et ses limites : lorsque l’HTA évolue depuis trop longtemps des lésions irréversibles s’installent au niveau rénal qui, même si elles n’impactent pas la fonction rénale, rendent inefficace l’angioplastie sur l’HTA.
Tian Y et al. Ann Vasc Surg 2021 ; doi: 10.1016/j.avsg.2021.06.042.
EVAR et SAR
La survenue d’une insuffisance rénale aigüe, dont la définition est variable, après EVAR est une complication encore fréquente (entre 2 et 18 % selon le contexte) et grave. Dans certaines situations la question du stenting concomitant (estimé à 3 % environ des EVAR) d’une artère rénale peut se poser pour traiter une sténose ou remonter la zone d’étanchéité (cheminée, par exemple). Ce travail se penche sur l’association EVAR + stenting des artères rénales (RAAS).
Méthodes
Analyse rétrospective de la base NSQIP (National Surgical Quality Improvement Program ; American College of Surgeons) sur la période 2011-2014. L’insuffisance rénale était définie par un DFG < 60 ml/min et l’insuffisance rénale aiguë (IRA) par une élévation de créatinine > 2 mg/dl.
Au total 6 183 patients avaient été identifiés. Un stenting de l’artère rénale avait eu lieu dans 281 cas (4,5 %). Le groupe EVAR + RAAS était caractérisé par un plus grand nombre de femmes (26 % vs 18 % ; p < 0,001), plus de patients avec un DFG préop < 60 ml/min (45 % vs 37 % ; p = 0,011), une extension plus distale vers les iliaques de l’anévrisme (p = 0,02). En postopératoire une IRA avait été plus fréquente dans le groupe EVAR + RAAS : 102 patients (dont 72 % avaient eu besoin d’une dialyse) (p = 0,002).
L’analyse par régression logistique a montré une association significative entre stenting rénal et IRA postopératoire (OR = 2,6 ; p = 0,003). Un DFG < 60 ml/min en préopératoire augmentait d’un facteur 6 le risque d’IRA postopératoire. Chaque augmentation de 1 cm du diamètre de l’anévrisme était responsable d’une augmentation de 17 % d’IRA postopératoire. Le risque de mortalité était multiplié par 22 en cas d’IRA postopératoire.
On note les limites de la base NSQIP (pas d’information sur l’indication du stenting : cheminée, sténose, décision peropératoire, etc.) malgré sa puissance. Ce travail identifie malgré tout clairement que les patients qui ont un stent rénal durant une procédure d’endoprothèse aortique constituent un sousgroupe à haut risque. Cela sous-entend qu’une préparation soigneuse (technique, hydratation) est indispensable pour limiter les complications, notamment emboliques et que l’indication doit être bien évaluée en préopératoire.
Nejim B et al. J Vasc Surg 2017 ; 65 (4) : 1080-8.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :


