Rythmologie et rythmo interventionnelle
Publié le 31 mai 2014Lecture 8 min
Fibrillation atriale et insuffisance cardiaque : quelle stratégie ?
J. SEITZ*, C. BARS** *Hôpital Saint-Joseph, Fédération de cardiologie, Marseille **Institut Mutualiste Montsouris, Hôpital Privé des Peupliers, Paris
La fibrillation atriale (FA) est le plus fréquent des troubles du rythme et représente un réel problème de santé publique. Cette maladie est en effet en pleine expansion avec le vieillissement de la population (prévalence européenne anticipée à 25 millions de patients en 2050).
L’insuffisance cardiaque voit également sa prévalence augmenter.
Contrairement à beaucoup de vieilles idées reçues, la FA est une maladie grave à ne pas négliger : cette maladie évolutive chronique est un facteur indépendant de mortalité(1).
Les causes de décès liée à la FA sont en majorité liées à l'insuffisance cardiaque
Dans une étude récente, E. Marijon et coll. ont étudié les différentes causes de mortalité dans une analyse rétrospective des données de l’étude RELY qui comprenait 18 113 patients ayant de la FA(2). Ils ont montré que la majorité des causes de décès dans cette population n’était pas liée à des accidents vasculaires cérébraux (ischémiques ou hémorragiques) mais à des morts de causes « cardiaques » (insuffisance cardiaque ou mort subite).
Dans ce travail qui ne comprenait que des patients ayant de la FA et correctement anticoagulés, le facteur prédictif indépendant de mortalité le plus fort était l’insuffisance cardiaque (IC).
Les patients qui mouraient avaient plus souvent une IC (NYHA III ou IV), une dysfonction VG (< 40 %), une cardiopathie d’étiologie ischémique et une hypertrophie VG.
Les progrès pharmacologiques et les études épidémiologiques réalisés dans le domaine des traitements anticoagulants ont permis d’obtenir un réel impact sur la mortalité par AVC (embolique ou hémorragique) et des bénéfices minimes sur la mortalité sont à attendre dans ce domaine dans les années à venir. Le plus grand challenge concernant la mortalité liée à la FA reste donc l’insuffisance cardiaque.
La FA est un facteur indépendant de mortalité, surtout chez l'insuffisant cardiaque
L’étude de Framingham en 1998 mettait en évidence une surmortalité des patients atteints de FA par rapport aux patients en rythme sinusal stable. Chez les patients déjà en IC, l’augmentation de mortalité liée à la FA a déjà été clairement démontrée(3).
La FA aggrave une insuffisance cardiaque préexistante et peut aussi en être la cause. Elle peut être responsable de cardiopathies rythmiques (largement sous-évaluées) avec ou sans cardiopathie préexistante(3,4). La FA est également responsable d’IC sur cardiopathie à fonction ventriculaire conservée (cardiopathies hypertrophiques le plus souvent), et son apparition correspond souvent à une étape critique dans l’évolution de ces cardiopathies(5).
Comment reconnaître une cardiopathie rythmique ?
Des patients porteurs de CMD « idiopathique » en FA dites « chroniques », correspondant à d’authentiques cardiopathies rythmiques, ne sont pas rares. Ces cardiopathies rythmiques sont diagnostiquées aujourd’hui car nous avons maintenant des moyens efficaces de maintenir le rythme sinusal des FA persistantes qui avaient échappé au traitement médical.
Une cardioversion électrique pour une FA, même ancienne, peut permettre d’apprécier une éventuelle amélioration clinique et de la fonction VG chez des patients qui s’étaient le plus souvent habitués à un état chronique d’asthénie et de limitation à l’effort.
Faut-il contrôler le rythme ou la fréquence ?
L’étude AFFIRM(6) datant de 2002, comparant la stratégie de contrôle de la fréquence cardiaque et la stratégie de maintien du rythme sinusal (par médicaments seulement) n’avait pas démontré de bénéfice dans les 2 groupes en termes de mortalité. Nombreux avaient alors été ceux qui tirait la conclusion (rapide) que seule la fréquence rapide était néfaste dans la FA et qu’essayer de maintenir le rythme sinusal n’avait pas d’intérêt.
En y regardant de plus près, on se rendait compte que 35 % des patients dans le groupe contrôle de la fréquence (censés être en FA) était en rythme sinusal et que 40 % des patients dans le groupe contrôle du rythme sinusal étaient en FA.
De plus, des analyses par groupe démontraient que le maintien du rythme sinusal était clairement associé à un meilleur pronostic : chez les septuagénaires(7), il diminuait significativement la mortalité et les hospitalisations, et chez les IC(8), il diminuait significativement les symptômes d’IC. Le rythme sinusal stable était associé clairement au meilleur statut fonctionnel. Ces auteurs concluaient que quand les médicaments étaient insuffisants pour maintenir le rythme sinusal, l’ablation de la FA (très peu développée à l’époque de l’étude) devait être envisagée maintenant chez ces patients avec IC.
Faut-il ablater la FA chez les patients insuffisants cardiaques ?
La FA comme l’asynchronisme ventriculaire peut être à la fois la cause d’une cardiopathie primitive et la conséquence aggravante d’une cardiopathie préexistante. La resynchronisation est connue aujourd’hui pour améliorer la fonction cardiaque, les symptômes et la survie. Malgré 25 à 30 % de non-répondeurs, cette technique est néanmoins aujourd’hui très largement utilisée à juste titre.
L’ablation de FA est une technique qui reste difficile, et d’autant plus chez les insuffisants cardiaques. Il s’agit souvent de FA persistantes sur des oreillettes dilatées et fibrosées. Mais d’après une métaanalyse portant sur 1 851 patients, l’ablation de FA dans l’IC est sûre et efficace (64 % à 96 % de patients sans arythmie après 1,4 procédure, 4 % de complications chez les patients avec ou sans IC)(9).
Comme dans toutes les FA dites « complexes » (FA persistantes le plus souvent), il est fréquent de devoir répéter les procédures pour obtenir un bon résultat (les reprises étant en général moins complexes). Dans cette même métaanalyse, les patients ayant une dysfonction VG avaient besoin de plus de séances d’ablation que les autres pour obtenir un bon résultat.
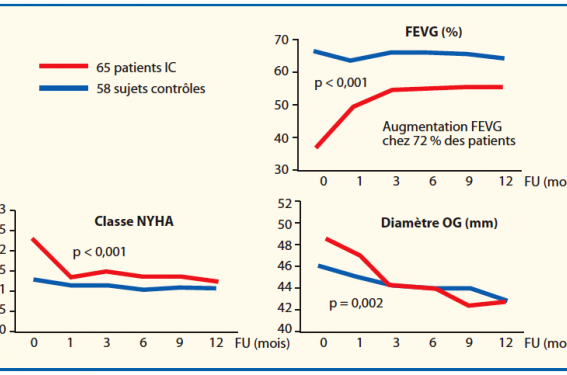
Néanmoins, différentes études ont montré l’amélioration de la FEVG, de la capacité d’effort et la qualité de vie chez des patients insuffisants cardiaques et ablatés d’un FA(5,9-11) (figure 1).
Figure 1. Amélioration fonctionnelle de la FEVG et diminution de la taille de l’oreillette gauche par ablation de FA chez des patients insuffisants cardiaques(10). D’après Hsu LF et al. NEJM 2014.
L’amélioration de la FEVG par ablation de FA est en moyenne de 11 %. Le bénéfice sur la mortalité est étudié actuellement dans l’étude CABANA (en cours). Malgré ces excellents résultats, la sélection des candidats à une ablation est indispensable, et les facteurs de mauvaise réponse à l’ablation doivent être connus (FA persistante de très longue durée, fibrose et dilatation très importante des oreillettes).
Ablation de FA ou ablation du nœud AV + stimulation biventriculaire ?
La stratégie de maintien du rythme sinusal est plus efficace que la stratégie de contrôle de la fréquence chez ce type de patients(8), mais les médicaments sont souvent inefficaces sur le long terme dans une stratégie comme dans l’autre.
Avant l’existence de l’ablation de la FA, chez des patients insuffisants cardiaques en FA réfractaire rapide, l’ablation du nœud AV associée à l’implantation d’un stimulateur était la seule option pour essayer de « stabiliser » ces patients. Aujourd’hui encore, dans les cas d’échec ou de non-indication d’ablation cette stratégie avec stimulation biventriculaire est utilisée pour limiter la désynchronisation induite par la stimulation, dangereuse chez ces patients en IC. Mais faut-il proposer aujourd’hui en 1re intention une ablation de FA ou une ablation du nœud AV associée à une stimulation biventriculaire ?
La stratégie d’ablation de FA a été comparée à la stratégie « ablation du nœud AV + pacemaker biventriculaire »(11) par l’équipe du Pr Michel Haissaguère : les résultats sont largement en faveur de l’ablation de la FA avec amélioration de la FEVG et de la capacité d’effort (figure 2). L’ablation du nœud AV associée à un PM doit être aujourd’hui réservée aux patients récusés pour une ablation.
Figure 2. L’étude PABA-CHF(11) a comparé la stratégie de contrôle de la fréquence efficace par ablation du nœud AV + stimulation biventriculaire à la stratégie de contrôle du rythme sinusal par ablation de la FA. Un bénéfice a été clairement démontré en faveur de l’ablation de FA avec amélioration de la FEVG et du test de marche.
Qui et quand ablater ?
Il n’existe pas de recommandations spécifiques concernant l’ablation de FA chez l’insuffisant cardiaque. D’après les recommandations actuelles, une ablation de FA doit être envisagée devant une FA symptomatique résistante au traitement médical.
Le bénéfice fonctionnel ainsi que sur la fonction cardiaque du maintien du rythme sinusal chez un patient insuffisant cardiaque (« systolique ou diastolique ») étant majeur, en cas d’échec des antiarythmiques, une ablation doit être envisagée en tenant compte du terrain : âge, ancienneté de la FA, sévérité de la cardiopathie, taille et fibrose de l’OG, etc.
Si une indication d’ablation est posée, le remodelage atrial induit par la FA elle-même justifie d’attendre le moins possible afin d’optimiser le résultat de celle-ci (ablation plus difficile avec de moins bons résultats dans les FA persistantes anciennes sur grosses oreillettes).
Comment ablater ?
L’ablation de FA compliquant une cardiopathie est souvent une ablation de FA difficile en raison d’un substrat arythmogène plus complexe que sur un cœur sain et doit être réalisée dans des centres « experts ». Les résultats décevants des protocoles anatomiques consistant à isoler les veines pulmonaires seulement dans les FA persistantes, ont poussé les électrophysiologistes à s’intéresser, non plus seulement aux veines pulmonaires, mais aux oreillettes. Dans un travail récent(12), nous avons montré que les veines pulmonaires pouvaient être passives dans la perpétuation de la FA, spécialement dans les FA persistantes et/ou sur des oreillettes dilatées et/ou avec dysfonction ventriculaire gauche. Des approches ciblant le substrat de la FA dans les oreillettes sont aujourd’hui de plus en plus utilisées (« défragmentation » seule(12,13) ou combinée à l’isolation des veines et la réalisation de « lignes »(14)) et donnent de bons résultats. L’objectif de telles procédures et de restaurer le rythme sinusal, voire d’obtenir une « non-inductibilité » (figure 3). Dans des cas particuliers de FA de très longue durée, sur très grosses oreillettes, une approche hybride chirurgicale épicardique mini-invasive et électrophysiologique (endocavitaire) peut également donner de bons résultats.
De nouveaux outils de cartographie de la FA nous permettront probablement d’être encore plus efficaces dans les années à venir.
Figure 3. Exemple d’un patient présentant une FA persistante depuis 9 mois ayant récidivé sous antiarythmique après plusieurs chocs électriques sur une cardiopathie dilatée à FEVG basse (35 %). L’ablation du substrat arythmogène de sa FA par défragmentation a permis de restaurer le rythme sinusal (haut de la figure) et d’obtenir la « non-inductibiité » (bas de la figure). L’origine rythmique de celle-ci est attestée par l’amélioration de sa FEVG (50 %) en rythme sinusal stable post-ablation à 6 mois.
En pratique
L’insuffisance cardiaque est la 1ere cause de mortalité chez les patients atteints de FA.
Elle peut être à l’origine d’une cardiopathie « rythmique » ou aggraver une cardiopathie préexistante (systolique ou diastolique).
La stratégie de contrôle du rythme sinusal doit clairement être une priorité tant que possible par rapport à la stratégie de contrôle de la fréquence. Le traitement médical optimal d’une cardiopathie préexistante peut en lui-même prévenir ou limiter les accès de FA.
En cas d’échec, du traitement médical de la cardiopathie et des antiarythmiques, l’ablation reste la seule option pour le maintien du rythme sinusal. Celle-ci est difficile et peut être réalisée en plusieurs temps, mais elle est efficace et sûre et doit faire partie aujourd’hui de l’arsenal thérapeutique de l’insuffisance cardiaque chez des patients bien selectionnés.
En collaboration avec : A. PISAPIA*, M. BREMONDY*, S. BEURTHERET*, A. FERRACCI*, J. FAURE*, E. PHILLIP*, P. KHANOYAN* *Hôpital Saint-Joseph, Fédération de cardiologie, Marseille **Institut Mutualiste Montsouris, Hôpital Privé des Peupliers, Paris
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :