Publié le 14 sep 2015Lecture 12 min
Épreuve d’effort dans le RAo serré asymptomatique
D. MALAQUIN, C. TRIBOUILLOY, CHU d’Amiens
Le rétrécissement aortique (RAo) est la valvulopathie la plus fréquente et sa prévalence augmente avec l’âge, estimée de 3 à 7 % chez les patients de plus de 65 ans. Le diagnostic est clinique et la sévérité est évaluée en échocardiographie. La majorité des patients sont asymptomatiques et la présence d’un RAo même modéré est associée à une surmortalité cardiovasculaire. Le suivi et la décision opératoire quand le RAo devient serré, chez ces patients, sont difficiles.
En effet, la mortalité opératoire, bien que faible, n’est pas nulle et on manque encore de données sur les déterminants de la progression de la sténose, les facteurs prédictifs de l’apparition d’une symptomatologie fonctionnelle et la stratification du risque. Actuellement, les experts européens recommandent le remplacement valvulaire aortique chez les patients porteurs de RAo serré avec symptômes (angor d’effort, syncope d’effort et dyspnée d’effort) ou en cas d’apparition d’une dysfonction VG de repos avec fraction d’éjection ventriculaire gauche (FEVG) < 50 % (recommandation de classe I)(1).
Clinique
Les symptômes initiaux sont souvent d’apparition progressive et insidieuse et peuvent être difficiles à reconnaître pour les patients. On estime qu’un tiers d’entre eux seraient en fait de « faux » asymptomatiques, diminuant inconsciemment leur activité physique pour éviter ou minimiser les symptômes. Cependant, l’apparition de ces symptômes marque un tournant évolutif dans la maladie avec une médiane de survie de 5 ans après la première crise d’angor, 3 ans après une première syncope et de 2 ans après l’apparition d’une dyspnée d’effort. On peut donc être tenté de proposer un remplacement valvulaire aortique (RVAo) précoce. Néanmoins, la mortalité opératoire actuelle du RVAo asymptomatique est estimée de 1 à 2 % et le patient après RVAo est exposé aux complications des prothèses valvulaires.
L’épreuve d’effort
Avec ou sans imagerie associée, strictement contre-indiquée chez les patients symptomatiques, l’épreuve d’effort est actuellement proposée dans les recommandations européennes(1) chez les asymptomatiques pour détecter les « faux asymptomatiques » et pour mieux stratifier les risques de mortalité sous traitement médical. Elle doit faire partie d’un algorithme décisionnel pour ces patients. Quand elle est couplée à l’imagerie, elle apporte des éléments supplémentaires sur la tolérance hémodynamique et ventriculaire gauche : gradient moyen à l’effort, FEVG et pression artérielle pulmonaire (PAPs) à l’effort. Quand elle est couplée à une mesure des échanges gazeux, el le permet d’évaluer l’adaptation cardio-pulmonaire à l’effort et donner une idée plus globale de la tolérance du RAo serré. L’épreuve d’effort est donc privilégiée par rapport aux tests pharmacologiques. Quand le test est couplé à l’échographie cardiaque, c’est l’exercice sur vélo semi-allongé per effort qui est recommandé avec mesures échocardiographiques avant, pendant et en fin d’effort. L’échographie d’effort pourrait avoir une valeur ajoutée par rapport au test d’effort « simple » chez les patients avec positivité électrique mais symptômes équivoques (cf. plus loin)(2-4).
Protocole recommandé
Quel que soit le type de test (avec imagerie ou sans), il est recommandé de pratiquer un protocole progressif, adapté à la performance attendue, permettant d’atteindre au moins 80 % de la fréquence maximale théorique (FMT) en l’absence de symptômes. Il est bien sûr, supervisé par une personne expérimentée.
Le test sur tapis roulant est préféré au Royaume-Uni et aux États-Unis alors que les Européens privilégient l’exercice sur vélo (qui permet de recueillir des paramètres échographiques pendant l’effort). Dans les recommandations américaines, c’est le protocole de Bruce modifié qui est pratiqué. L’exercice commence par un échauffement de 2 minutes à 25 watts, incrémenté par paliers de 25 watts toutes les 2 minutes. Un protocole d’incrément de 10 watts est plus approprié chez les patients âgés avec faible niveau d’activité de manière à obtenir plus souvent les 80 % de la FMT souhaités. Dans notre centre, nous utilisons un protocole de 10 watts/minute en rampe chez ce type de patients. Bien sûr les contre-indications habituelles doivent être respectées (tableau 1) : RVAo serré symptomatique, hypertension artérielle de repos non contrôlée, arythmie symptomatique ou non contrôlée au repos, incapacité physique (ce qui n’est pas rare chez le sujet âgé) ou mentale à comprendre et à réaliser le test.
Épreuve d’effort standard
Le test est interrompu en cas d’atteinte de la FMT ou en cas d’apparition de symptômes : angor typique, dyspnée limitante, lipothymie ou malaise, hypotension marquée (de plus de 20 mmHg par rapport au niveau de départ), sous-décalage horizontal ou descendant de plus de 2 mm par rapport au niveau de base ou arythmie ventriculaire significative (c’est-à-dire tachycardie ventriculaire soutenue ou salves ventriculaires de plus de 3 ESV).
L’apparition de ces symptômes lors du test d’effort prédit dans plusieurs études le développement des symptômes dans la vie quotidienne, le risque de mort subite et la nécessité à court terme de RVAo au cours du suivi, en particulier chez les patients les plus jeunes et les plus actifs(5). Dans une métaanalyse récente, en cas d’épreuve d’effort anormale, le risque d’événement cardiaque au cours du suivi est multiplié par 8 et le risque de mort subite par 5. Cependant il faut distinguer la valeur prédictive des critères cliniques, électriques et hémodynamiques. L’étude de l’équipe de Das(5) a montré par exemple, que sur une série de 125 RAo asymptomat iques tes tés à l’effort, la valeur prédictive négative d’une épreuve d’effort normale était de 87 % pour l’apparition de symptômes pendant les 12 mois suivants. Dans cette série, le sous-décalage du segment ST et la réponse tensionnelle anormale (définie dans sa série par la non-élévation de pression artérielle à l’effort) n’apportaient pas statistiquement de bénéfice par rapport au critère apparition des symptômes seul pour prédire l’apparition d’événements au cours du suivi. Le critère électrique de sous-décalage ne doit donc pas justifier un arrêt du test s’il est isolé et modéré. En effet, l’hypertrophie ventriculaire secondaire au RAo donne souvent des troubles de repolarisation difficiles à interpréter dès le repos, une coronaropathie pouvant être également associée rendant le test électriquement positif. Dans la série de Das, le test était arrêté logiquement si le sous-décalage isolé dépassait 5 mm. L’interprétation des symptômes seuls n’est pas toujours facile chez les personnes âgées. En effet, dans la même étude, la valeur prédictive positive d’un test d’effort pathologique pour l’apparition spontanée de symptômes dépend de l’âge (57 % sur toute la série versus 79 % chez les moins de 70 ans actifs physiquement). Le type de symptômes donne également des informations différentes. Sur la cohorte entière, 83 % des patients présentant une lipothymie à l’effort deviennent spontanément symptomatiques durant le suivi de 12 mois, contre 50 % des patients avec angor et 54 % des patients avec dyspnée. Il faut dire que chez les plus âgés, il est difficile de faire la part des choses entre une insuffisance respiratoire, un déconditionnement ou une dyspnée liés uniquement au RAo.
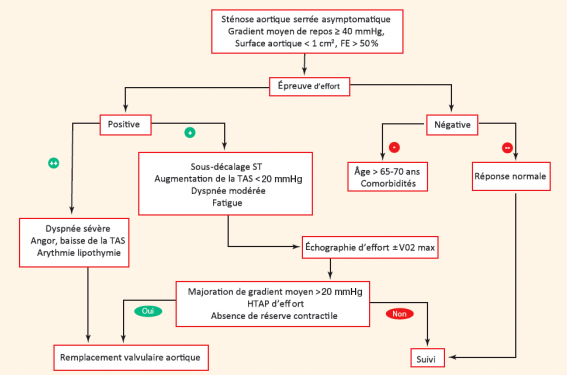
On pourrait donc distinguer des critères de positivité « franche » (dyspnée majeure, arythmie, lipothymie, chute tensionnelle) et des critères de positivité « intermédiaire » (absence d’élévation tensionnelle, franc sous-décalage ST, dyspnée modérée et fatigue) pour aider à la décision (figure 1).
Dans ces situations intermédiaires, l’épreuve d’effort couplée à l’imagerie (échographie d’effort) ou à une mesure de la VO2 peut heureusement apporter des éléments complémentaires objectifs importants.
Figure 1. Place des examens à l’effort dans le RAo. Adapté de J. Magne et coll.(3).
Échocardiographie d’effort
L’examen nécessite entraînement et matériel spécifique (ergomètre semi-allongé). Les acquisitions se font tout au long de l’examen à tous les stades en se concentrant sur les paramètres valvulaires (gradient moyen transaortique et vitesses sous-aortiques), ventriculaires gauches (FEVG et strain) et sur les pressions (PAPs et pressions de remplissage VG) (figure 2)(2,4,6).
Figure 2. Protocole d’échographie d’effort et paramètres à recueillir. Adapté de C. Henri et coll.(6).
Pressions de remplissage En début d’effort, on s’efforce de recueillir le E/E’ en Doppler pulsé et DTI avant la fusion de E et A qui survient en général vers 100 bpm.
Gradient transvalvulaire Au cours de l’effort, on recueille en Doppler continu le flux transaortique et l’évolution du gradient moyen. Il doit être acquis à chaque stade de l’examen, car il existe des réponses biphasiques. Quel que soit le résultat du test, une augmentation supérieure ou égale à 18-20 mmHg du gradient moyen est associée à un excès d’événement cardiaque durant le suivi. Dans une série multicentrique de 2010(4), sur 186 patients asymptomatiques (avec épreuve d’effort « classique » normale), une augmentation de plus de 20 mmHg de gradient moyen transaortique est associée à une majoration du risque d’événement cardiaque de 3,8, indépendamment de l’âge, de la fonction VG ou du gradient de repos. Ce critère apporterait une valeur pronostique supplémentaire par rapport aux données échographiques de repos et aux critères ECG d’effort. En effet, l’augmentation du gradient à l’effort refléterait la sévérité de la sténose aortique au repos et le caractère « rigide » de la valve aortique qui est non compliante et dont la surface d’ouverture n’augmente pas à l’effort. Ceci pourrait être lié au caractère calcifié de la valve, ce qui est un marqueur de risque important du pronostic dans le RAo.
Il faut cependant interpréter les variations de gradient en fonction des variations de volume d’éjection systolique (VES). En effet, une faible variation de VES peut entraîner une grande variation de gradient sur une valve très calcifiée, puisqu’elle n’a pas de « réserve » d’ouverture. On peut observer également une telle majoration de gradient sur une valve avec « réserve » d’ouverture, simplement liée à une grande majoration du VES, le pronostic n’étant pas du tout le même dans ces deux cas de figure. Des réponses biphasiques peuvent être observées sur le gradient, raison pour laquelle il faut s’efforcer de le recueillir à chaque stade. En effet, au cours de l’effort la réserve contractile s’exprime pour augmenter le VES de manière à s’adapter à la demande périphérique croissante. Quand ce premier mécanisme arrive à son maximum, c’est l’augmentation de fréquence cardiaque qui participe à cette majoration du VES. Or, sur un ventricule gauche hypertrophié (réactionnel au RAo) et donc peu compliant, cette tachycardie peut devenir délétère par perte de la phase diastolique de remplissage et le gradient peut secondairement s’abaisser dans la phase ultime de l’effort.
Variations de la fonction VG et réserve contractile L’étude de la « fonction VG » est nécessaire à chaque stade de l’effort. On s’efforcera d’apprécier la fonction VG globale, mais aussi segmentaire, pour détecter une éventuelle coronaropathie associée. L’absence de réserve contractile, définie par l’absence ou la quasiabsence d’élévation de FEVG lors de l’effort, voire sa diminution, est associée à l’apparition de symptômes d’effort et d’événements cardiaques durant le suivi. En effet, elle marquerait déjà un stade plus avancé de la maladie avec dommage myocardique et un certain degré de fibrose qui limiterait la compliance VG et ne permettrait plus une adaptation correcte entre la demande périphérique et l’élévation du débit cardiaque. La fonction VG peut également être estimée par le Doppler tissulaire. L’équipe de Van Pelt a suggéré qu’une élévation à l’effort de l’onde S’ supérieure à 5 cm/s à l’effort, serait une bonne valeur pour déterminer la présence de réserve contractile. Le 2D speckle tracking utilisé par l’équipe de Donal est une technique d’évaluation de la fonction VG plus séduisante. Une augmentation inférieure à -1,4 % du strain global longitudinal à l’effort serait associée à une dysfonction VG latente et à une réponse anormale à l’effort. Des travaux sont encore nécessaires pour confirmer l’intérêt en pratique clinique du Doppler tissulaire et du 2D strain à l’effort.
Valeur et variation de PAPs Le gradient transtricuspide est recueilli en Doppler continu au repos et quand cela est possible à tous les stades de l’effort. Une élévation rapide des gradients et des Vmax tricuspides est associée à une absence d’adaptation vasculaire pulmonaire avec faible compliance pulmonaire et élévation rapide des résistances vasculaires pulmonaires. Au repos, une hypertension artérielle pulmonaire (HTAP) > 50 mmHg est associée à un plus mauvais pronostic avec une mortalité postopératoire plus importante. Une HTAP d’ effort (PAP s > 60 mmHg) serait un facteur prédictif d’apparition d’HTAP de repos et de symptômes. Le risque d’événement cardiaque dans les 3 ans serait multiplié par 2 en cas d’HTAP d’effort chez les patients asymptomatiques avec FEVG conservée(7).
Cependant ce paramètre doit être interprété avec du recul car il est très dépendant des conditions de charge, de l’âge de la tension artérielle de repos et de son évolution au cours de l’effort, du sexe, de l’évolution du débit cardiaque à l’effort, de la fonction ventriculaire droite ainsi que du niveau de charge fourni. On sait qu’il peut exister chez des patients sans cardiopathie sous-jacente une élévation de la PAPs à l’effort supérieure à 60 mmHg lors d’un effort prolongé et soutenu(8). C’est plutôt la rapidité d’apparition de l’HTAP au cours de l’effort que son niveau, qu’il faudrait prendre en considération.
VO2 max et RAo asymptomatique
L’épreuve d’effort cardio-pulmonaire apporte, dans notre expérience, des éléments objectifs très informatifs pour caractériser l’étiologie de l’intolérance à l’effort et/ou de la dyspnée. Le résultat permet d’apprécier la capacité de l’organisme, en particulier du coeur, des poumons et des vaisseaux à assurer le transport de l’oxygène et l’élimination du CO2. Cependant, alors que de nombreuses études ont validé le test dans le cadre de l’insuffisance cardiaque, il y a encore peu de données sur le RAo asymptomatique. Il a été montré que le pic de VO2 était significativement plus bas chez les patients avec RAo asymptomatique que chez des patients contrôles. Dans une série de 43 RAo asymptomatiques à l’interrogatoire de notre centre(9), un pic de VO2 < 14 ml/kg/min et une pente VE/VCO2 > 34 sont apparus associés à la survenue de symptômes lors du test d’effort et donc à une indication opératoire. L’avantage de ce dernier paramètre est qu’il soit déductible d’un test d’effort sous maximal et donc indépendant de la motivation du patient.
Impact sur la décision clinique
Chaque paramètre recueilli à l’effort apporte donc des éléments pronostiques résumés dans le tableau 2 :
• Les recommandations de RVAo selon les experts européens(1) sont essentiellement basées sur la « simple » épreuve d’effort et sont fortes pour indiquer le RVAo en cas d’apparition de symptômes d’effort (classe I) alors qu’elles sont plus modérées en cas de chute tensionnelle (sous le niveau de repos) (classe IIa).
• En cas de réponses équivoques (sous-décalage ST, dyspnée modérée, fatigue ou absence d’élévation tensionnelle) ou d’épreuve d’effort négative dans le cas de patients de plus de 65- 70 ans (chez qui les symptômes sont plus difficiles à mettre en évidence du fait de tests moins poussés en charge), on pourrait proposer la réalisation d’une échocardiographie d’effort ou d’une épreuve d’effort cardiorespiratoire en complément. Le paramètre échographique d’élévation de gradient de plus de 20 mmHg est une recommandation de l’ESC plus faible de RVAo (classe IIb). L’apparition d’une HTAP d’effort et l’absence de réserve contractile ne font pas l’objet d’une recommandation ESC spécifique mais paraît apporter une valeur pronostique supplémentaire.
• On notera que toutes ces recommandations sont basées sur les avis d’experts, toutes de niveau de preuve C. L’algorithme décisionnel proposé par J. Magne et coll. est présenté sur la figure 1. Notons que les recommandations ACC/AHA n’intègrent pas l’écho d’effort (tableau 2)(10).
• En l’absence de signes de mauvaise tolérance à l’effort, le suivi clinique est de mise, rapproché tous les 3 à 6 mois. Néanmoins une Vmax au repos supérieure à 5,5 m/sec et une progression franche Vmax transvalvulaire de plus de 0,3 m/sec/an associée à des calcifications importantes sont des paramètres qui peuvent justifier d’une indication de RVAo en classe IIa chez les patients à faible risque opératoire et avec performance d’effort normale(1).
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :
Articles sur le même thème
publicité
publicité