Valvulopathies
Publié le 02 mar 2018Lecture 7 min
Prise en charge des patients valvulaires asymptomatiques - Intérêt des centres-experts médico-chirurgicaux
Jean-Luc MONIN, Institut des Maladies Valvulaires/Institut Mutualiste Montsouris, Paris

La prise en charge des patients valvulaires asymptomatiques pose un certain nombre de problèmes au cardiologue clinicien : tout d’abord évaluer précisément la sévérité de l’atteinte valvulaire et son retentissement cardiaque, s’assurer ensuite du caractère réellement asymptomatique de cette valvulopathie et enfin peser le rapport bénéfice/risque d’une éventuelle intervention. Ces difficultés justifient pleinement l’existence des centres d’expertise pour les maladies valvulaires (Heart Valve Centers), qui regroupent les différentes spécialités médicochirurgicales (cardiologues cliniciens et interventionnels, chirurgiens cardiaques, anesthésistes, imageurs) et permettent une prise en charge multidisciplinaire optimale de ces patients. L’intérêt et le prérequis de ces centres experts sont largement abordés dans les recommandations européennes (ESC-EACTS) sur la prise en charge des patients valvulaires réactualisées en 2017(1).
Étape clinique
L’interrogatoire du patient est essentiel afin de rechercher d’éventuels symptômes potentiellement liés à l’atteinte valvulaire et de lister les antécédents et comorbidités extracardiaques. L’auscultation cardiaque et un examen cardiovasculaire complet sont incontournables pour évaluer la sévérité d’une atteinte valvulaire et son retentissement cardiaque, pulmonaire et veineux. Le ressenti du patient et son souhait par rapport à une éventuelle intervention sont également des données fondamentales.
Échocardiographie/scanner/IRM cardiaque
L’échocardiographie est l’examen clé pour quantifier la sévérité d’une valvulopathie et son retentissement hémodynamique. La quantification d’une valvulopathie repose toujours sur l’intégration de plusieurs paramètres qualitatifs et quantitatifs, parmi lesquels les indices de taille et de fonction ventriculaire gauche, l’estimation du débit cardiaque et des pressions pulmonaires et la fonction ventriculaire droite sont particulièrement importants. Les principaux critères de sévérité des régurgitations valvulaires sont rappelés tableau 1. En cas de discordance entre les différents critères échocardiographiques, l’IRM cardiaque occupe actuellement une place importante, notamment comme méthode de référence pour le calcul des volumes et de la fraction d’éjection ventriculaire gauche(2). Entre des mains entraînées, l’IRM cardiaque de flux est également très fiable pour calculer la fraction de régurgitation en cas d’insuffisance aortique et à moindre degré en cas d’insuffisance mitrale primaire(2). Les intérêts du scanner cardiaque sont multiples : calcul du score calcique valvulaire en cas de difficultés d’évaluation d’un rétrécissement aortique(3), mesure précise des différents diamètres de l’aorte thoracique, anatomie des artères coronaires et des abords vasculaires potentiels en cas de procédure interventionnelle envisagée.
Tests d’effort/2D-strain/peptides natriurétiques
L’épreuve d’effort simple est recommandée dans la plupart des valvulopathies pour s’assurer du caractère réellement asymptomatique chez un patient donné et quantifier l’adaptation cardiovasculaire à l’effort. L’intérêt de l’échographie d’effort est beaucoup plus limité, elle a d’ailleurs disparu des recommandations ESC-EACTS en 2017(1). Le niveau de recommandations de l’échographie d’effort était déjà faible en 2012 (classe IIb)(4), et le niveau de preuve scientifique reposait essentiellement sur quelques études dont les effectifs dépassaient rarement la centaine de patients.
En l’absence de nouvelle publication depuis 2012, le consensus d’expert de 2017 a donc décidé de ne pas recommander l’usage de l’échographie d’effort en cas de rétrécissement aortique ou d’insuffisance mitrale asymptomatique.
L’étude de la fonction longitudinale ventriculaire gauche en échographie transthoracique (2D-strain) semble intéressante sur le plan physiopathologique : en cas de rétrécissement aortique sévère, il a été démontré que la diminution du strain sur les segments basaux et moyen du ventricule gauche était corrélée à la présence d’une fibrose myocardique(5), elle-même corrélée à une valeur pronostique péjorative y compris après remplacement valvulaire(6). Malgré cela, le niveau de preuve scientifique est encore trop faible pour recommander l’utilisation du 2D-strain, notamment pour influencer une décision thérapeutique.
Les peptides natriurétiques ont été mieux traités par le comité des guidelines 2017 avec, actuellement, une recommandation de classe IIa en faveur de la chirurgie pour un taux de BNP supérieur à 3 fois la normale pour l’âge, en cas de rétrécissement aortique asymptomatique(1).
À l’opposé, l’usage du BNP n’est pas mentionné en cas d’insuffisance aortique ou mitrale, les études étant beaucoup moins nombreuses par comparaison au rétrécissement aortique.
Insuffisance aortique : intérêt de la chirurgie conservatrice
Dans les pays industrialisés, les principales causes d’insuffisance aortique chronique sont actuellement les maladies dégénératives de la valve, qu’elle soit bicuspide ou tricuspide et les anévrismes de l’aorte initiale. De ce fait, l’insuffisance aortique touche volontiers des sujets jeunes, n’ayant pas atteint l’âge de 60 ans, à partir duquel l’implantation d’une bioprothèse est recommandée par les Guidelines(1).
Une des principales nouveautés des Guidelines 2017 est la recommandation (classe I) d’évaluation collégiale dans un centre d’expertise valvulaire pour les patients jeunes, susceptibles de bénéficier d’une chirurgie conservatrice de la valve aortique(1).
Il est précisé que les meilleurs candidats sont les patients dont la valve aortique reste souple, sans calcification, qu’elle soit bicuspide ou tricuspide, avec comme mécanisme principal de l’insuffisance aortique un prolapsus de sigmoïde (figure 1) ou un anévrisme de la racine aortique (figure 2).
Une 2e recommandation de classe I est en faveur des techniques chirurgicales de réimplantation ou de remodelage de la racine aortique associés à une annuloplastie externe (intervention de Yacoub modifiée par Lansac) en cas d’anévrisme de la racine aortique chez un patient jeune, adressé à un chirurgien expérimenté pour ce type d’intervention(1). Par ailleurs, les seuils décisionnels pour proposer une intervention au stade asymptomatique en cas de dilatation sévère du ventricule gauche ou de l’aorte initiale n’ont pas été modifiés.
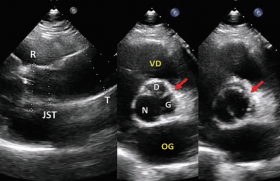
Figure 1. Prolapsus de sigmoïde coronaire droite. A. Échographie transthoracique, parasternale longitudinale + zoom : décrochage en « marche d’escalier » du bord libre de la sigmoïde coronaire droite (flèche). B. Schéma correspondant : le jet d’insuffisance aortique tombe verticalement vers la valve mitrale antérieure, la zone de convergence (PISA) est souvent exploitable dans cette incidence. Ao = racine aortique ; VG = ventricule gauche.
Figure 2. Anévrisme de la racine aortique dans le cadre d’une maladie de Marfan. Échographie transthoracique, parasternale longitudinale : la racine aortique (sinus de Valsalva) est dilatée en « bulbe d’oignon » et mesure 50-51 mm de diamètre maximal, d’où une indication chirurgicale de classe I.
La chirurgie doit être envisagée en cas d’insuffisance aortique sévère/asymptomatique et en l’absence de dysfonction systolique VG, si le diamètre télédiastolique VG dépasse 70 mm ou si le diamètre télésystolique dépasse 50 mm (25 mm/m2).
Les seuils à partir desquels une intervention préventive est recommandée en cas d’anévrisme de l’aorte proximale sont rappelés tableau 2.
a. Antécédent familial de dissection aortique ou antécédent personnel de dissection artérielle, insuffisance aortique ou mitrale sévère, désir de grossesse, hypertension artérielle ou augmentation de taille de l’aorte > 3 mm en 1 an, mesurée par la même technique d’imagerie et confirmée par une 2e technique (scanner synchronisé à l’ECG de préférence). b. Un seuil abaissé à 40 mm peut être envisagé en cas de petit gabarit, notamment chez la femme, dans les mutations TGFBR2 ou les syndromes de Loeys Dietz avec signes extracardiaques sévères. c. Un seuil plus bas peut être considéré en cas de petit gabarit, notamment chez la femme.
Rétrécissement aortique : HTAP et BNP plasmatique
La principale nouveauté concernant les patients asymptomatiques ayant un rétrécissement aortique sévère est une indication de classe IIa en faveur d’une intervention en cas d’hypertension artérielle pulmonaire sévère, définie par une PAPS > 60 mmHg au repos, confirmée par un cathétérisme droit et sans autre cause d’HTAP.
Rappelons que des taux élevés de BNP plasmatique (> 3 fois la normale pour le sexe et l’âge) sont également en faveur d’une intervention en cas de rétrécissement aortique sévère asymptomatique (classe IIa). Par ailleurs, concernant le choix entre une intervention chirurgicale ou une prothèse transcathéter (TAVI), les guidelines insistent à nouveau sur l’importance des centres experts (Heart Valve Centers) qui doivent regrouper impérativement un service de chirurgie cardiaque et un service de cardiologie médicale et interventionnelle. En effet, seule une collaboration structurée sous la forme de staffs multidisciplinaires (Heart Valve Team) permet d’optimiser le meilleur choix thérapeutique pour un patient donné.
Insuffisance mitrale primaire : diamètre télésystolique VG
Concernant l’insuffisance mitrale primaire, dont la principale cause dans les pays industrialisés est actuellement le prolapsus valvulaire, l’échographie d’effort a également été retirée des recommandations 2017(1). Le faible niveau de preuve scientifique et l’absence de nouvelles données depuis 2012 justifient ce retrait. Concernant les seuils décisionnels sur la taille du ventricule gauche en cas d’insuffisance mitrale sévère asymptomatique, les Européens considèrent toujours qu’un diamètre télésystolique > 45 mm est en faveur d’une dysfonction systolique VG et justifie donc une indication opératoire de classe I. Une des nouveautés de ces guidelines 2017 et le glissement progressif vers le seuil de 40 mm de diamètre télésystolique, considéré par les Américains : chez un patient asymptomatique qui présente une insuffisance mitrale sévère et une fraction d’éjection préservée (> 60 %), un diamètre télésystolique VG entre 40 et 44 mm, associé à un faible risque opératoire et une forte probabilité de plastie mitrale réalisée dans un centre expert est en faveur d’une chirurgie précoce, au même titre qu’une dilatation importante de l’oreillette gauche (volume OG indexé > 60 ml/m2) (classe IIa)(1).
En pratique
La prise en charge des patients asymptomatiques atteints d’une valvulopathie sévère reste un challenge pour le cardiologue clinicien, malgré les performances des différents examens complémentaires et l’amélioration des techniques chirurgicales et interventionnelles.
L’évaluation précise de la sévérité de l’atteinte valvulaire, du retentissement cardiaque et de l’adaptation cardiovasculaire à l’effort nécessitent une collaboration étroite entre les différents experts : cardiologues cliniciens, imagerie cardiovasculaire invasive et non invasive, chirurgiens cardiaques et anesthésistes.
Le rôle du staff multidisciplinaire (Heart Valve Team) est donc incontournable afin de garantir la meilleure prise en charge pour un patient donné, grâce à une évaluation rigoureuse du rapport bénéfice/risque tout en tenant compte des souhaits du patient et de sa famille.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :