Publié le 01 juin 2018Lecture 5 min
EKOS : la solution dans l’embolie pulmonaire de risque intermédiaire haut ?
Laurent BONELLO1 et coll.*, Département de cardiologie, Hôpital Universitaire Nord, Marseille
De nouvelles techniques de prise en charge invasive des embolies pulmonaires les plus sévères ont montré des résultats encourageants. Parmi celles-ci, la thrombolyse in situ dirigée par les ultrasons est un outil particulièrement efficace et innovant. Elle pourrait transformer la prise en charge initiale des EP à risque intermédiaire haut d’une attitude attentiste à une prise en charge permettant de réduire drastiquement le risque d’évolution défavorable — sans le sur-risque hémorragique associé à la thrombolyse systémique.
L’embolie pulmonaire est une pathologie dont la fréquence ne cesse de croître et dont la morbi-mortalité reste élevée faute d’évolution thérapeutique notable. Depuis 2014, les recommandations européennes ouvrent la voie à l’utilisation de nouveaux outils dans les formes les plus sévères afin de réduire le risque d’évolution vers le choc cardiogénique ou le décès(1,2). Parmi ces innovations, la thrombolyse in situ guidée par les ultrasons représente une thérapeutique particulièrement intéressante(3).
Cas clinique
Une patiente âgée de 80 ans, active et en excellent état général, est admise aux urgences pour un épisode de syncope à son domicile. Elle se plaint depuis lors d’une dyspnée de repos. Elle est hypertendue et a pour principal antécédent une embolie pulmonaire non provoquée survenue 4 ans auparavant. Le traitement anticoagulant a été interrompu par son cardiologue il y a 6 mois.
À l’admission, la patiente présente une pression artérielle à 100/60 mmHg, une fréquence cardiaque à 115 bpm et une saturation à 95 % sous 10 L d’O2. Elle ne présente aucun signe de choc par ailleurs ni de phlébite clinique. Sa gazométrie témoigne d’un effet shunt. Les lactates artériels sont à 2 mmol/L. L’électrocardiogramme retrouve une tachycardie sinusale associée à des ondes T négatives dans le territoire antérieur.
L’échocardiographie transthoracique retrouve une dilatation ventriculaire droite (VTSVD 58 mL et VTDVD 85 mL) associée à une dysfonction systolique sévère TAPSE à 13 et une onde S à 5,65 cm/s. Les PAPs sont évaluées à 78 mmHg. On note une fonction systolique ventriculaire gauche normale mais on constate la présence d’un septum paradoxal.
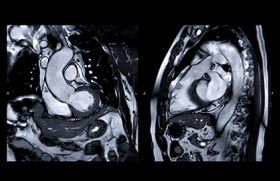
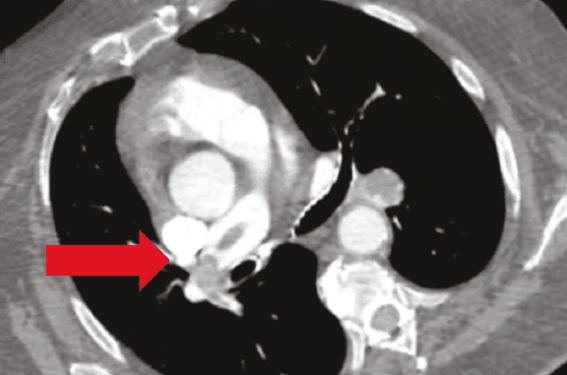
La suspicion d’embolie pulmonaire est rapidement confirmée par un angioscanner qui montre une embolie pulmonaire bilatérale proximale avec une dilatation VD et un rapport VD/VG > 1,3 (figure 1A et B).
Figure 1. A. Thrombus proximal AP gauche. B. Thrombus proximal AP droite. C. Injection sélective montrant un volumineux thrombus dans l’AP gauche. D. Injection sélective montrant un thrombus occlusif dans l’AP droite.
La biologie confirme l’embolie pulmonaire de gravité intermédiaire haute avec une troponine IC à 0,5 μg/L (99e percentile 0,05) et un BNP à 1 800. On note par ailleurs une légère insuffisance rénale aiguë ainsi qu’une cytolyse (3 fois la normale) associée à une cholestase (bilirubine à 25).
La patiente est hospitalisée en unité de soins intensifs de cardiologie où elle bénéficie de la mise en place d’héparine non fractionnée par voie intraveineuse. Le Doppler veineux retrouve une TVP gauche poplitée.
Au cours des 12 premières heures, la patiente présente une aggravation de sa détresse respiratoire avec un PAO2 à 75 mmHg sous 30 L/d’O2 et une tachypnée à 35/min. Il n’existe pas de signe de choc malgré une PA limite à 110/55 mmHg chez cette patiente hypertendue. Du point de vue biologique, on note une augmentation des lactates à 3 mmol/L.
Il est décidé devant cette dégradation sous traitement et au vu du terrain qui est associé à un risque hémorragique élevé (âge élevé, sexe féminin, faible poids), ainsi qu’à l’absence de signe de choc, de réaliser une thrombolyse in situ dirigée par les ultrasons.
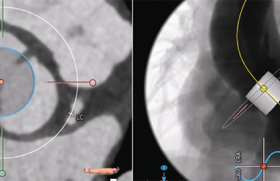
Après un abord veineux fémoral à l’aide de 2 introducteurs de 6Fr, une mesure invasive des PAP est réalisée et retrouve des PAPs à 90 mmHg. Une angiographie pulmonaire sélective retrouve à gauche un thrombus volumineux à l’origine de l’AP s’étendant jusqu’aux artères sous segmentaires du lobe inférieur et à droite un arrêt net du produit de contraste au niveau du tronc de l’AP (figure 1C et D).
La procédure comprend le franchissement du thrombus à l’aide de guides et de cathéters conventionnels puis la mise en place du cathéter EKOS de thrombolyse in situ dirigée par les ultrasons avec une zone de traitement de 12 cm. Le dispositif est mis en place dans chaque artère pulmonaire avec sa portion distale située dans l’artère lobaire inférieure (figure 2). La procédure se déroule sans difficultés.
Figure 2. Cathéter EKOS en place.
La thrombolyse est réalisée sur une durée de 10 heures avec l’injection d’1 mg/heure d’actilyse (altéplase) sur chaque cathéter.
Un monitoring toutes les 2 heures de l’ETT est réalisé afin de suivre l’évolution des PAPs ainsi que de la fonction systolique ventriculaire droite.
On note 2 heures après le début de la thrombolyse in situ une réduction de l’oxygéno-dépendance de la patiente. L’échographie cardiaque quant à elle retrouve une réduction de la dilatation VD, ainsi que de la dysfonction VD chez une patiente dont les PAPs ont régressé pour atteindre 60 mmHg. À l’issue de la thrombolyse (H+10), 20 mg d’actilyse ont été administrés, l’oxygénothérapie est réduite à 3 L/min pour une saturation à 95 %. La patiente est eupnéique sans signe de choc. Sa PA s’est normalisée à 140/80 mmHg.
Le bilan biologique témoigne d’une normalisation de la troponinémie et d’une réduction du BNP. Les fonctions rénales et hépatiques sont en voie de normalisation. L’échographie cardiaque transthoracique montre une dysfonction VD modérée avec une réduction du rapport VD/VG mesuré à 1, un TAPSE à 15 et une vitesse de l’onde S mesurée à 8,5. Les PAPs sont estimées à 40 mmHg. La patiente est transférée en unité d’hospitalisation conventionnelle où un relais par rivaroxaban est réalisé. Eu égard à cette récidive d’événement thromboembolique veineux sans facteur déclenchant retrouvé, il lui sera recommandé de poursuivre son traitement anticoagulant oral à vie.
Discussion
Ce cas clinique illustre l’intérêt de la prise en charge invasive des EP de risque intermédiaire haut. La thrombolyse in situ guidée par les ultrasons permet de réduire très rapidement les pressions pulmonaires et la dysfonction VD, réduisant ainsi le risque d’aggravation de l’état hémodynamique de ces patients ainsi que la durée de leur surveillance aux soins intensifs. Cette technique extrêmement simple sur le plan procédural peut être réalisée par un cardiologue interventionnel en 30 minutes.
De plus, cette « thrombolyse facilitée » permet de diviser par 5 la dose de thrombolytique utilisée comparativement à une thrombolyse conventionnelle par voie intraveineuse (20 mg versus bolus de 10 mg d’actilyse puis infusion de 90 mg en 2 heures). Cependant, le prix élevé des cathéters ne permet pas à l’heure actuelle de proposer cette thérapeutique innovante à tous les patients présentant une EP à risque intermédiaire haut. La mise en place de ce dispositif au décours d’un processus de sélection des patients les plus à risque de dégradation sur les critères cliniques, gazométriques, biologiques et échographiques devrait permettre d’améliorer leur pronostic et d’en accroitre le rapport coût/efficacité.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :
Articles sur le même thème
publicité
publicité