Congrès et symposiums
Publié le 01 mar 2020Lecture 7 min
Les AOD dans la maladie coronaire : des études randomisées à la vraie vie
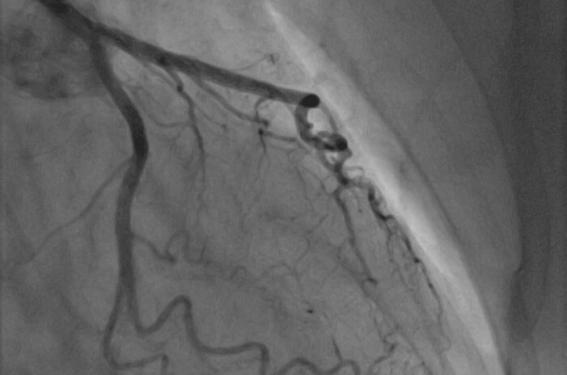
La prévalence de la fibrillation atriale augmente avec l’âge et coexiste souvent avec la maladie coronaire. Cette situation fréquente nécessite d’adapter la stratégie thérapeutique pour prévenir le risque ischémique sans augmenter le risque hémorragique, après un événement coronarien aigu. Tous les anticoagulants bloquent la formation de thrombine — qui est aussi un activateur plaquettaire — et par là, sont complémentaires des antiagrégants plaquettaires. Le concept émergent vise à agir sur ces deux composants, la thrombine et l’activation plaquettaire en combinant un anticoagulant à un antiagrégant plaquettaire.
Plusieurs essais réalisés chez des patients coronariens revascularisés par endoplastie et ayant une fibrillation atriale (AF) ont montré un meilleur bénéfice/risque (réduction des événements hémorragiques) avec une stratégie comportant un anticoagulant oral direct (AOD) comparativement à un anti-vitamine K (AVK) en association au traitement antiplaquettaire. Les résultats de l’étude AUGUSTUS montrent la supériorité de l’apixaban vs AVK et la supériorité de la bithérapie sur la trithérapie sur le critère principal (événements hémorragiques). Le meilleur bénéfice/risque est obtenu avec la bithérapie comparativement à la trithérapie : moins d’événements hémorragiques et d’hospitalisations sans surcroît d’événements ischémiques.
FA + revascularisation coronaire : quel traitement antithrombotique ?
Cette situation clinique complexe oblige à prendre en considération trois concepts : le traitement préventif des complications thromboemboliques (TE) de la FA, où les anticoagulants sont plus efficaces que la bithérapie antiplaquettaire ; le traitement préventif des complications coronaires ischémiques, en particulier la thrombose de stent, où la bithérapie antiplaquettaire fait mieux que les anticoagulants ; l’association obligatoire de ces traitements devant résulter en un risque de complications hémorragiques acceptable, en sachant que la trithérapie comporte un sur-risque hémorragique majeur (x 2 ou 3, vs traitement antithrombotique simple), en particulier au cours des 3 premiers mois. Ce surrisque hémorragique est associé à un sur-risque de mortalité hospitalière (x 2-3) dû à la majoration du risque ischémique et thrombotique consécutif à l’arrêt du traitement. Quelle solution thérapeutique ?
Dans le cadre d’une association antithrombotique, l’utilisation du prasugrel en trithérapie augmente notablement (x 4) le risque hémorragique. Ni le ticagrelor ni le prasugrel ne sont recommandés dans cette situation.
La bithérapie antithrombotique associant un anticoagulant et un antiagrégant plaquettaire est plus efficace que la trithérapie, avec une diminution d’environ 60 % du risque hémorragique et thrombotique. Une réduction de la durée de la trithérapie peut être envisagée (6 semaines au lieu de 6 mois dans ISAR-Triple), pour réduire le risque de thrombose sans augmenter le risque hémorragique.
La troisième stratégie intègre les deux précédentes et fait appel aux nouvelles molécules, un AOD associé au traitement antiplaquettaire en bithérapie, éventuellement un inhibiteur de P2Y12, le clopidogrel dans la majorité des cas ; cette stratégie est associée à une diminution des complications comparativement à la trithérapie, sans signal d’augmentation des thromboses de stent. Cette stratégie a été testée dans PIONEER et REDUAL, mais ces deux études n’avaient ni la puissance statistique ni le design pour trancher la question de savoir si la réduction des complications hémorragiques observée avec la bithérapie était liée au traitement AOD ou à la non-utilisation de la trithérapie. D’où l’intérêt de l’étude AUGUSTUS qui a inclus un nombre bien supérieur de patients et a utilisé un plan factoriel autorisant une double randomisation : apixaban pleine dose vs AVK ou aspirine vs placebo, chez des patients ayant bénéficié d’une angioplastie et tous recevant un inhibiteur de P2Y12 pendant au moins 6 mois. Les patients sous trithérapie avaient un sur-risque de 89 % sans qu’il y ait dans cette étude de signal péjoratif en termes de décès chez les patients sous bithérapie. Il n’y a pas de différence significative en termes de décès cardiovasculaire ou autre, IDM, AVC, thrombose de stent, revascularisation urgente, mais un signal indiscutable en faveur d’un sur-risque en termes de thrombose de stent dans le groupe bithérapie sur un taux d’événements très bas (0,5 % dans le groupe aspirine, 0,9 % dans le groupe placebo), vs trithérapie habituelle. Dans ce contexte, l’apixaban fait un peu mieux que les AVK.
Le nombre de patients à traiter (NNT) pour éviter une thrombose de stent avec une trithérapie par rapport à une bithérapie à 6 mois est de 222 ; le NNT qui va poser une complication hémorragique avec une trithérapie est de 41 versus bithérapie. Au total, le prix à payer pour éviter 1 thrombose de stent est de 6 complications hémorragiques cliniquement pertinentes. Une métaanalyse des essais évaluant ces stratégies de traitement confirme les résultats de l’étude AUGUSTUS.
Dans les précédentes recommandations de l’ESC, la bithérapie anticoagulant + antiplaquettaire était réservée aux patients à haut risque hémorragique alors que les patients à risque thrombotique et ischémique élevé justifiaient d’une trithérapie de 1 à 6 mois, alors que les recommandations américaines considéraient d’emblée une bithérapie AOD + inhibiteur P2Y12, l’aspirine devant s’envisager dans l’environnement du geste d’angioplastie à la phase aiguë d’hospitalisation, voire un peu plus longtemps ; la trithérapie pendant 1 mois permet de couvrir le risque de thrombose de stent chez les patients à haut risque. La stratégie européenne pour les patients coronariens chroniques considère aujourd’hui qu’au décours d’une angioplastie non compliquée, l’interruption de l’aspirine peut être considérée en deçà de la première semaine et que la trithérapie (1 mois ou un peu plus) doit être réservée aux patients à haut risque de thrombose de stent et bas risque hémorragique. Le ticagrelor ou le prasugrel ont une place en bithérapie (sans aspirine en raison du surrisque hémorragique).
Quelles sont les leçons des registres dans la FA ?
Nous disposons de deux registres français, PAROS et NAXOS.
Le premier est un registre transversal multicentrique non interventionnel réalisé en 2016 à la demande des autorités de santé auprès d’un échantillon de cardiologues, afin de caractériser les populations traitées par apixaban et les conditions d’utilisation du traitement, pendant 3 mois. Les patients pouvaient recevoir un AOD ou un AVK ; devaient être inclus les 6 derniers patients traités par apixaban, les 3 derniers par un autre AOD et les 3 derniers patients traités par AVK. Il s’agit d’une population âgée (73 ans en moyenne). Les patients initiés sous AVK sont les plus âgés, les plus graves et avec le plus de comorbidités (17 % ont une insuffisance rénale sévère ou terminale vs 2 % recevant l’apixaban, aucun ne recevant les deux autres AOD). Le deuxième groupe le plus grave est celui recevant de l’apixaban ; ceux recevant du dabigatran ou du rivaroxaban sont un peu moins âgés, moins graves et avec moins de comorbidités. La même distribution que celle observée pour l’insuffisance rénale est notée pour le score CHA2DS2-Vasc (60 % des scores ≥ 4 sous AVK, 43 % sous apixaban, 38 % sous les deux autres AOD) ou le score HAS-Bled ou le score de Charlson.
En analyse multivariée, trois facteurs sont prédictifs de l’utilisation de l’apixaban de préférence aux autres AOD : la fonction rénale, l’existence d’un diabète et la prescription par un cardiologue. Comparativement aux AVK, l’apixaban est prescrit à des patients moins fragiles, ayant moins d’insuffisance rénale et moins à risque de saignement.
La deuxième étude NAXOS, longitudinale, collaborative française visait à étudier la prescription en vie réelle de l’apixaban et à la comparer à celle des autres anticoagulants oraux dans la FA, chez les patients naïfs de traitement anticoagulant, et de mesurer la sécurité et la mortalité toutes causes. La première comparaison oppose apixaban et AVK, la deuxième concerne l’apixaban vs autres AOD disponibles en France. NAXOS s’est appuyé sur les données du SNIRAM et a utilisé une cohorte de patents de ≥ 18 ans débutant un traitement anticoagulant oral pour FA, entre janvier 2014 et décembre 2016. L’étude a utilisé des scores de propension afin de comparer les patients. Au total plus de 410 000 patients ont été inclus dans l’étude (21 % de la cohorte initiale).
Un quart des patients reçoivent un AVK, 87 000 de l’apixaban, 21 000 du dabigatran et 100 000 du rivaroxaban. Les caractéristiques des patients selon les sous-groupes d’anticoagulation sont équivalentes à celles observées dans PAROS. Pour l’apixaban comme pour le rivaroxaban, les deux tiers des patients reçoivent la pleine dose, un tiers une dose réduite ; 42 % des patients sous dabigatran reçoivent la dose de 150 mg x 2/j, 35 % celle de 100 mg x 2/j, 3 % la dose réduite de 75 mg x 2/j. La mortalité est de 12 % dans le groupe AVK, vs 3,7-3,8 % dans les groupes AOD. De nombreux patients (8 %) vont changer de traitement durant la période de l’étude ou l’arrêter (42 % l’AVK, 23 % l’apixaban, 33 % le dabigatran et 32 % le rivaroxaban). La fréquence des arrêts de traitement, d’autant plus élevée que les patients sont âgés, illustre bien les difficultés d’adhérence au traitement anticoagulant.
Les taux d’hémorragies majeures sont importants, comme ceux des AVC (3 % sous AOD, 6 % sous AVK). En ajustant les comparaisons, l’apixaban est associé à un risque hémorragique ayant conduit à l’hospitalisation moindre de moitié vs AVK, également plus faible que sous dabigatran. En termes d’efficacité, le risque d’AVC et d’embolie systémique est plus faible sous apixaban vs AVK et équivalent à celui du rivaroxaban ou du dabigatran. La mortalité est plus basse sous apixaban vs AVK et rivaroxaban, et non différente sous apixaban vs dabigatran.
Ces résultats ont été répliqués avec quatre autres méthodes d’ajustement pour tous les critères de jugement. Malgré la force de cette étude, il faut tenir compte des limites inhérentes à la méthodologie d’une étude observationnelle. Néanmoins, la concordance des résultats de NAXOS avec les données des essais cliniques est rassurante quant à la sécurité et à l’efficacité de l’apixaban.
D’après un symposium BMS/Pfizer avec la participation de R. Storey, N. Meneveau et P.G. Steg
JESFC 2020
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :