Cardiologie interventionnelle
Publié le 03 mai 2011Lecture 7 min
ACC - Une édition riche en informations pour le cardiologue interventionnel
B. CHEVALIER, Centre cardiologique du Nord, Saint Denis

Le remplacement valvulaire aortique transcutané (« TAVI » des Anglo-Saxons) présenté en primeur juste après le discours officiel d’ouverture du président de l’ACC, des résultats à un an de la cohorte A de PARTNER. Rappelons pour mémoire que la cohorte B (358 patients) randomisait des patients porteurs de sténose aortique récusés pour la chirurgie classique entre TAVI (Valve Sapien-Edwards*) et traitement dit médical. Les résultats (TCT 2010 et publication préalable dans le New England Journal of Medicine) signaient le couronnement du TAVI avec un gain de 20 % en valeur absolue sur la mortalité à un an, du jamais vu en cardiologie interventionnelle !
PARTNER
Le TAVI est conforté en tant qu’alternative valide dans la sténose aortique à haut risque…
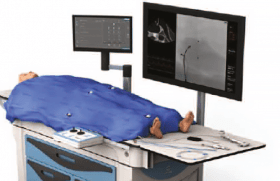
(figure 1)
La cohorte A randomisait 699 patients à haut risque chirurgical (STS score > 10) entre le TAVI (transfémoral ou à défaut transapical) et le remplacement valvulaire conventionnel. Le critère primaire était la non-infériorité du TAVI sur la mortalité à 1 an de toute cause, critère qui a été atteint puisque celle-ci est de 24,2 % contre 26,8 %. Le bras transfémoral, critère secondaire principal préspécifié, sépare un peu plus les deux courbes : 22,2 % versus 26,4 % pour le RVA mais l’étude ne prévoyait pas de tester la supériorité. Cardiologues et chirurgiens ont remarquablement travaillé avec des mortalités à « 30 jours » (mais décomptées à partir de la randomisation et non de l’intervention, donc minorées par un délai randomisation-intervention de plus de 10,6 jours pour le TAVI et de 15,6 jours pour la chirurgie !) de 3,4 % et 6,5 %. Ce résultat est d’autant plus satisfaisant que certaines équipes avaient une expérience fort limitée du TAVI avant le début de l’étude. Sans surprise, il y a plus de fibrillations auriculaires et de saignements majeurs en chirurgie et plus de complications vasculaires en transcutané ; il faut se souvenir que les Américains n’ont accès qu’au système de pose initial nécessitant un abord vasculaire de 22 ou 24 French.
Figure 1. Implantation transapicale de valve Sapien-Edwards en salle hybride (ICPS Massy).
Mais l’étude soulève également des questions non résolues
Le risque exact d’AVC, ici plus élevé dans le groupe TAVI (8,3 % versus 4,3 %, p = 0,04) et supérieur aux publications antérieures.
Néanmoins, ceci inclut les AIT et il faut tenir compte du suivi neurologique spécialisé de tous les patients qui a certainement permis de détecter des lésions cérébrales qui passent inaperçues dans certaines séries. La différence n’est pas significative pour les AVC majeurs. Le mécanisme est certainement embolique au cours de la procédure mais il existe également des AVC tardifs. Faut-il screener plus attentivement les patients en termes de lésions carotidiennes, d’athérome friable de l’arche aortique et orienter alors ces patients vers d’autres voies ? Certainement. Faut-il évoquer le rôle de la courbe d’apprentissage (qui allonge les procédures), de l’anesthésie générale encore largement utilisée alors qu’elle est rarement nécessaire ? Probablement. Faut-il développer de systèmes de protection cérébrale ? Il est encore trop tôt pour le dire. Quel est le risque de thrombose sur les mailles du stent ? Difficile à évaluer car nous manquons d’études anatomiques.
L’impact réel des fuites paravalvulaires qui sont plus fréquentes après TAVI.
En effet, le différentiel initial de mortalité s’accroit en faveur du TAVI jusqu’à 6 mois puis les courbes convergent à nouveau pour se rejoindre presque à 12 mois.
Faut-il y voir le rôle d’un résultat hémodynamique insuffisant, laissant des patients avec des fuites intermédiaires à importantes, dont on sait qu’elles sont mal tolérées en cas de dysfonction VG préalable ?
Une mortalité élevée en transapical, numériquement supérieure à la chirurgie sans possibilité de faire des tests statistiques vu la taille de l’échantillon (207 patients au total). On en dira certainement ce qui s’est dit pour PARTNER Europe : cette voie sélectionne des patients plus fragiles. Au-delà, il y a certainement un point d’interrogation quant à l’avenir de cette voie, ce qui conduit les chirurgiens à développer des substituts : abord chirurgical sous-clavier ou abord aortique direct.
Un taux d’embolisation de valve faible (2,6 %) mais néanmoins inhabituel, possible reflet de la courbe d’apprentissage.
Enfin, bien sûr, on ignore dans quelle mesure ces résultats sont extrapolables à l’autre valve transcutanée (Medtronic Corevalve*) qui diffère sensiblement par son concept et sa technique de pose.
La publication complète, retardée pour éviter la surprise de la cohorte B (le NEJM l’avait envoyé par internet à tous ses correspondants la veille de la présentation en late breaking trial), sera nécessaire pour mieux comprendre. D’ici là le message reste largement positif puisque des équipes peu entraînées, utilisant un système de pose obsolète, font aussi bien que le remplacement valvulaire traditionnel chez ces patients à haut risque.
Un petit mot de l’étude médico-économique de la cohorte B : elle évalue à 50 200 $ le coût d’un an de vie gagnée avec le TAVI. Les auteurs placent cela au même niveau que la resynchronisation dans l’insuffisance cardiaque et 30 % en dessous l’hémodialyse chronique.
EVEREST II
Dans le domaine valvulaire, les résultats à deux ans d’EVEREST II, sont venus tempérer l’enthousiasme de l’an passé, en matière de réparation mitrale percutanée. La comparaison randomisée à la chirurgie a tendance à tourner en faveur de celle-ci puisque le taux d’événements (décès, chirurgie mitrale, IM au moins grade III) n’y est de 27 % contre 45 % pour le Mitraclip. Il est difficile d’imaginer que le gain en termes de sécurité immédiate de l’intervention, essentiellement due à un moindre recours à la transfusion, contrebalance une technique dont les indications sont encore floues, l’efficacité inférieure et qui, par ailleurs, vise à reproduire un geste chirurgical (l’Alfieri) dont l’intérêt est encore largement débattu. Le sous-groupe des régurgitations fonctionnelles a de meilleurs résultats sans que l’on sache s’il y a un bénéfice clinique à les corriger. Cette publication a relancé les sceptiques : ceux qui pensent que la chirurgie restera reine comme ceux qui croient que la solution viendra du remplacement mitral percutané, encore en phase de développement.
Une chose est sûre : seuls les patients ayant une IM importante avec une contre-indication chirurgicale sont des candidats validés pour cette technique.
ABSORB
Du côté des coronaires, le stent actif est le grand pourvoyeur d’essais cliniques. D’abord sa version « tout absorbable », à travers les résultats à un an de la cohorte B de l’étude ABSORB qui confirme des résultats angiographiques identiques aux stents actifs les plus récents (Perte tardive à un an de 0,27 mm versus 0,23 mm pour le Xience). Les étapes ultérieures du suivi clinique et par imagerie multimodalités (échographie, OCT, scanner coronaire) (figure 2) permettront d’évaluer les bénéfices potentiels par rapport à un dispositif permanent : récupération de la vasomotricité et de la conformabilité déjà mis en exergue, remodelage artériel positif et régression de la plaque athéromateuse suggérés par les premières études d’imagerie à 2 ans.
Figure 2. Endoprothèse active absorbable (implantation et au suivi à 2 ans) en imagerie par OCT.
Études de stenting
Dans ce flot incessant d’études de stenting, je retiens trois études importantes :
ISAR-CABG évalue, chez 610 patients porteurs de sténose de pontage veineux, le rôle du stent actif : réduction de 50 % des revascularisations sans effet sur les critères de sécurité. Cette indication du stent actif, jusque-là floue, est maintenant validée, même si l’angioplastie de ces lésions se raréfie.
L’étude PRECOMBAT randomise 600 patients porteurs de sténose du tronc commun, le plus souvent pluritronculaires (Syntax score moyen 25) entre angioplasties au Cypher versus pontages. Malgré une chirurgie plus moderne que Syntax (64 % off pomp, 2,1 greffons artériels/patient), le stent fait jeu égal à 2 ans sur les critères de sécurité et, même s’il y a plus de revascularisations (9 versus 4,2 %), le critère de non-infériorité sur les événements cardio-cérébraux est atteint (différence 2 %). Cette étude souligne la question du stent choisi dans Syntax et donc les limites d’en extrapoler les résultats à des endoprothèses plus performantes.
Elle conforte le classement II de l’angioplastie du tronc commun dans les récentes recommandations européennes.
L’étude EXCELLENT teste l’hypothèse de 6 mois de bithérapie antiplaquettaire (après stent actif) versus le classique 12 mois des recommandations nord-américaines : jeu égal total à un an sur les critères cliniques de sécurité et d’efficacité ainsi que sur le risque hémorragique et la thrombose tardive. Seul sous-groupe à bénéficier des 12 mois de traitement : les diabétiques. La sous-randomisation entre Cypher* et Xience* influe peu sur les résultats avec une petite tendance en faveur des 12 mois en cas d’usage du stent de première génération.
RIVAL
Enfin, terminons en notant que nos collègues américains découvrent le rôle de l’abord radial à travers l’étude RIVAL qui est en fait le pooling de deux études sous-dimensionnées. Au-delà des limites méthodologiques, on y trouve la réduction de la mortalité pour cette voie (1,3 % vs 3,2 %) dans l’angioplastie primaire et le rôle majeur du volume de procédures radiales réalisés dans chaque centre sur le bénéfice clinique. Au-delà de 146 angioplasties radiales/opérateur/an, non seulement les complications vasculaires sont très largement diminuées mais aussi le risque de décès/infarctus/AVC est significativement réduit.
OSCAR
L’étude OSCAR (Hisao Ogawa) compare un traitement par ARA2 à forte dose (olmésartan 40 mg) à un traitement par olmésartan 20 mg associé à un inhibiteur calcique dans la prévention CV chez 1 164 hypertendus à risque (de 65 à 84 ans) qui, sous olmésartan 20 mg/j, gardent une PAS ≥ 140 mmHg et/ou une PAD ≥ 90 mmHg, et ayant au moins un facteur de risque associé.
Le critère principal est la somme des événements CV mortels ou non. Durant l’étude, la PA est significativement moindre sous l’association, avec 70,7 % contre 62,8 % de patients à l’objectif tensionnel. Les résultats montrent une équivalence globale entre les 2 stratégies avec une petite prime pour les AVC avec l’association, récompensant une PA plus observée.
L’analyse en fonction de la préexistence ou non d’une pathologie cardio-vasculaire montre que le bénéfice de l’association est essentiellement survenu en cas de maladie cardio-vasculaire préalable : RR 1,63, p = 0,0261. La différence de PA entre les deux groupes durant l’étude ne permet pas de savoir si l’éventuel bénéfice est à attribuer aux traitements reçus ou au seul effet tensionnel.
Ainsi, il semble bien que de fortes doses d’ARA2, ici l’olmésartan, sont efficaces en prévention primaire, en particulier chez les diabétiques, très représentés ici. Une fois les maladies CV déclarées (souvent des coronaropathies), les inhibiteurs calciques semblent avoir leur place.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :