Insuffisance cardiaque
Publié le 18 nov 2008Lecture 9 min
L'IC à fonction systolique préservée : en quoi est-elle différente de l'IC systolique?
A. MEIZELS, L. HITTINGER, J.-L. DUBOIS-RANDÉ, T. DAMY, Hôpital Henri Mondor, Créteil
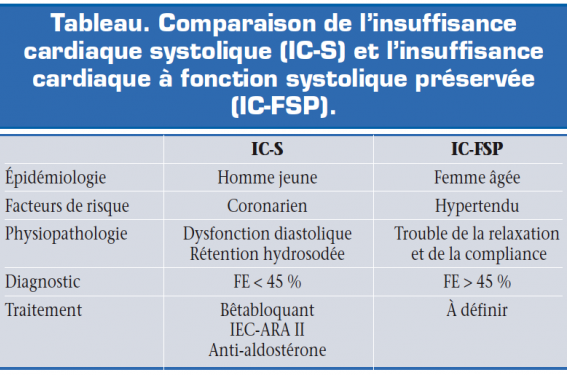
L’insuffisance cardiaque (IC) est divisée classiquement en deux entités : l’insuffisance cardiaque systolique (IC-S) ou à fraction d’éjection altérée et l’insuffisance cardiaque à fonction systolique préservée (IC-FSP). Longtemps considérée comme une pathologie rare, l’IC-FSP représente aujourd’hui, selon les études récentes, environ 50 % des insuffisances cardiaques. Mais son diagnostic reste complexe et son traitement mal défini contrairement à l’IC-S, ce qui se traduit par une mortalité inchangée depuis 20 ans, contrairement à celle de l’IC-S qui est en réduction constante. Il est donc important de concentrer nos efforts sur l’amélioration du diagnostic et du traitement de l’IC-FSP pour réduire sa mortalité.
Définition
L’insuffisance cardiaque se définit comme l’incapacité du ventricule gauche (VG) à assurer dans des conditions normales le débit de sang nécessaire aux besoins métaboliques et fonctionnels de l’organisme. Elle se traduit cliniquement par une dyspnée et une asthénie.
Physiopathologie
L’insuffisance cardiaque systolique est définie comme une altération de la fraction d’éjection du ventricule gauche en dessous de 45 %. Elle est liée à une défaillance de la pompe cardiaque secondaire à une altération primitive du myocarde (cardiopathie ischémique, myocardiopathie) ou d’une surcharge mécanique liée à un obstacle ou surcharge volumétrique (cardiopathie valvulaire, hypertensive, congénitale). Les patients présentent un remodelage excentrique aboutissant à une augmentation du volume de la cavité du VG et des anomalies de la fonction cardiaque prédominant sur la performance systolique et la contractilité. La pression diastolique du VG est augmentée alors que la rigidité passive de la paroi du VG est normale ou diminuée. Elle entraîne l’activation de mécanismes neurohormonaux engendrant une rétention hydrosodée responsable des signes cliniques (œdèmes).
L’IC-FSP est définie par l’association d’un syndrome clinique d’insuffisance cardiaque avec une fraction d’éjection normale ou > 45 %. Pour la Société européenne de cardiologie, la présence d’une anomalie de la fonction diastolique du VG est également nécessaire alors que, pour les recommandations américaines, cette condition n’est pas obligatoire. En effet, des anomalies de la fonction diastolique sont fréquemment mais inconstamment mises en évidence dans l’IC-FSP.
Le remplissage diastolique dépend de deux propriétés du ventricule gauche :
- d’une part, de la relaxation, processus actif du cardiomyocyte, correspondant à la fin de l’éjection (phase de relaxation isovolumique et remplissage rapide),
- d’autre part, de la compliance ou rigidité, processus passif (remplissage lent).
Le remplissage diastolique dépend également de la contraction atriale qui survient en fin de diastole. Les anomalies diastoliques peuvent donc être liées à une atteinte de la relaxation par atteinte du cardiomyocyte et une rigidité accrue par atteinte du tissu de soutien (fibrose, etc.). Elles sont responsables de l’élévation des pressions de remplissage.
Les paramètres de la fonction systolique comme la performance, la fonction et la contractilité paraissent normaux (FEVG) mais comportent un certain degré d’altération (infra-clinique). C’est la survenue de phénomènes aigus tels qu’une surcharge de pression (poussée hypertensive) ou une perte de la systole auriculaire (passage en ACFA) qui vont décompenser la cardiopathie sous-jacente. Enfin, en comparaison à l’IC-S, la rétention hydosodée est souvent moindre, voire absente.
Épidémiologie
Les patients atteints d’IC-FSP sont généralement plus âgés, plus souvent de sexe féminin, hypertendus, ayant des troubles du rythme auriculaire et moins souvent atteints de coronaropathie que ceux avec une IC-S. Le diabète et l’obésité sont également des facteurs de risque reconnus mais de manière moins établie (tableau).
Diagnostic
Le diagnostic de l’insuffisance cardiaque repose sur des symptômes cliniques, des examens biologiques (BNP) et surtout l’échographie cardiaque.
Les signes fonctionnels sont très peu spécifiques du type d’IC (S ou FSP). Ces symptômes sont l’asthénie (fréquente chez le sujet âgé) et la dyspnée, auxquels peuvent s’associer des signes physiques de décompensation (crépitants, œdèmes des membres inférieurs, galop, turgescence jugulaire, reflux hépato-jugulaire, etc.). La distinction entre IC-S et IC-FSP reste impossible par ces seules données cliniques.
Alors que pour l’IC-S, la mesure d’une fraction d’éjection abaissée à l’échographie cardiaque suffit pour affirmer le diagnostic, pour l’IC-FSP, l’établissement du diagnostic est plus difficile. En effet, toute dyspnée avec une FE normale n’est pas forcément une IC-FSP. Peu d’éléments à l’ECG ou à la radio du thorax permettent de différencier l’IC-S de l’IC-FSP, ces derniers ayant toutefois plus souvent une hypertrophie électrique.
BNP. De nombreuses études ont montré l’intérêt du dosage du BNP pour établir le diagnostic, évaluer le pronostic et le suivi du patient insuffisant cardiaque. Il a surtout une grande valeur prédictive négative, un BNP < 100 (ou NT-proBNP < 300 pg/ml) éliminant une origine cardiaque à des symptômes évocateurs. Les IC-FSP ont habituellement des taux de BNP moins élevées comparativement aux IC-S, cette caractéristique ne permettant toutefois pas de les différencier en pratique quotidienne.
L’écho-Doppler cardiaque est l’examen clef en pratique clinique, permettant de différencier IC-FSP et IC-S. Une fraction d’éjection abaissée à < 45 % affirme le diagnostic d’IC-S. Elle doit être mesurée par la méthode de Simpson biplan, méthode de référence. L’estimation visuelle est moins précise. L’utilisation de la méthode tridimensionnelle peut améliorer la précision du calcul.
L’autre intérêt majeur de l’échographie est l’étude de la fonction diastolique et la mise en évidence d’une élévation des pressions de remplissage du VG, critère majeur du diagnostic. Cette appréciation est fondée sur l’analyse du flux mitral en Doppler pulsé (E/A), complétée par la mesure des vélocités à l’anneau mitral en Doppler tissulaire (Ea), par la mesure du flux Doppler dans la veine pulmonaire (onde A mitrale Am), ou encore par la mesure en mode TM et Doppler couleur de la vitesse de propagation du flux de remplissage protodiastolique dans le VG (onde Vp).
Ainsi, un rapport E/A inversé, un Ea < 8 cm/s et une onde Vp < 35 cm/s sont en faveur d’un trouble de la relaxation. Des rapports E/Ea > 15, E/Vp > 2,5 et Ap-Am > 30 ms sont en faveur de pressions de remplissage élevées.
Un rapport E/Ea < 8 et Ap–Am négatif permet de conclure à des pressions normales, des valeurs intermédiaires ne permettent pas de conclure. Dans ces deux derniers cas, il peut être difficile d’affirmer le diagnostic (IC-FSP améliorée par le traitement ou erreur initiale au diagnostic). L’échographie peut alors mettre en évidence des critères indirects comme une hypertrophie ventriculaire gauche (masse VG > 125 g/m2 chez l’homme, 110 g/m2 chez la femme), présente dans 40 à 60 % des cas ou une dilatation de l’oreillette gauche (volume > 29 ml/m2) qui reflètent une élévation des pressions auriculaires. Dans certains cas on peut aussi utiliser l’échographie d’effort qui peut montrer une élévation anormale des pressions à l’effort et/ou une élévation du rapport E/Ea.
Ainsi, un rapport E/Ea > 13 à l’effort est spécifique d’une élévation anormale des pressions de remplissage.
Le cathétérisme cardiaque reste l’examen de référence pour affirmer le diagnostic d’IC-FSP en montrant une élévation des pressions de remplissage ventriculaire gauche. Il est probablement sous-utilisé et est actuellement réservé au diagnostic difficile de l’IC-FSP.
Le diagnostic d’IC-FSP reste donc difficile, contrairement à l’IC-S, avec des signes cliniques très peu spécifiques, et repose donc surtout sur l’échographie cardiaque. Il a été mis en place des algorithmes pour aider au diagnostic. La complexité du diagnostic peut en partie expliquer la mortalité encore élevée.
Mortalité et pronostic
La plupart des études semblent montrer que la mortalité de l’IC-S est légèrement plus importante que celle de l’IC-FSP (10-15 % vs 5 à 8 % par an). Dans l’étude CHARM, la mortalité annuelle était de 10 % dans le bras IC-S et de 5,4 % dans le bras IC-FSP. Dans le registre de la Mayo Clinic, allant de 1987 à 2001, 47 % des IC hospitalisées avaient une FE conservée et la dernière analyse récemment publiée montre une mortalité à 1 an de 29 % pour les ICD contre 32 % pour les IC-S et de 65 vs 68 % à 5 ans. Les auteurs de ces registres montraient que, contrairement à l’IC-S, la mortalité de l’IC-FSP n’a pas diminué au cours de ces 20 dernières années.
On peut noter que le traitement des patients avec une IC-FSP à la sortie de l’hôpital semble moins optimal en termes de prévention que ceux avec une IC-S.
L’étude de Bhatia montre que le taux de réadmissions à 30 jours et à un an pour décompensation cardiaque sont identiques entre les deux groupes.
Il a aussi été montré qu’il existe des facteurs de mauvais pronostic dans l’IC-FSP. L’étude de O’Connor (optimise HF) a identifié quelques indicateurs indépendants de mortalité. Ainsi, un âge avancé, le diabète, l’existence d’une coronaropathie, la présence de signes cliniques d’insuffisance cardiaque étaient associées à une augmentation de la mortalité.
Le Digitalis Investigation Group Trial décrit comme principaux indicateurs d’une mortalité accrue l’insuffisance rénale, des symptômes de classe III ou IV de la NYHA, le sexe masculin et l’âge. Il est probable qu’une amélioration de la prise en charge de ces facteurs pronostiques (diabète, maladie coronaire) pourrait améliorer la mortalité.
Traitement
Contrairement à l’IC-S, peu d’études ont été réalisées dans l’IC-FSP. De ce fait, il n’existe pas de recommandations spécifiques sur l’utilisation systématique d’une classe thérapeutique particulière dans l’IC-FSP. Selon les dernières recommandations nationales éditées par la Société française de cardiologie, le traitement de l’IC-FSP demeure empirique (classe IIa, niveau de preuve C).
Seuls deux essais (CHARM et PEP CHF) visant à évaluer l’efficacité d’un bloqueur du système rénine-angiotensine-aldostérone (candésartan, perindopril) ont été publiés, ne montrant pas un réel bénéfice sur le pronostic vital. Cependant les effets reconnus des médicaments utilisés dans l’IC-S (ARA II, IEC, antialdostérone et bêtabloquants) sur le remodelage du ventricule gauche, sur la fibrose myocardique, sur l’allongement du temps de remplissage ou sur l’ischémie myocardique, suggèrent un bénéfice potentiel de ces mêmes molécules dans l’IC-FSP. On attend les résultats de l’étude I-PRESERVE.
Dans l’étude SENIOR-HF publiée récemment, le nébivolol a montré une amélioration de la mortalité et des taux de réadmission chez les patients dont environ un tiers avaient une IC-FSP. Toutefois, la sous-étude échocardiographique n’a pas noté de modification des paramètres échocardiographiques dans ce sous-groupe.
Le traitement des facteurs étiologiques reste donc essentiel pour prévenir les poussées d’insuffisance cardiaque et l’aggravation de la maladie. Ainsi, l’utilisation des antihypertenseurs permet, en abaissant la postcharge, d‘améliorer la relaxation et le remplissage du VG. Tous les antihypertenseurs peuvent être utilisés, mais en cas d’hypertrophie ou de remodelage du VG, il est recommandé d’utiliser ceux qui font régresser la masse du VG. La revascularisation coronarienne en cas de cardiopathie ischémique et le traitement chirurgical des valvulopathies sévères sont évidemment nécessaires, même s’il n’existe pas de données démontrant une amélioration de la dysfonction diastolique.
Il est aussi nécessaire de limiter les facteurs déclenchants des décompensations cardiaques, comme l’ACFA, la poussée hypertensive, et l’ischémie myocardique. Le traitement et la prévention des troubles du rythme auriculaire sont essentiels, le remplissage du VG étant assuré essentiellement par la contraction auriculaire. La poussée hypertensive est un grand pourvoyeur de décompensation cardiaque de l’IC-FSP. Chez ces patients, le traitement diurétique, utile au début de la prise en charge, doit être rapidement réduit, voire interrompu, en fonction de la présence ou non de rétention hydrosodée associée. En effet, le VG étant peu compliant, le maintien des diurétiques peut entraîner une baisse excessive de la précharge, réduisant le volume d’éjection, à l’origine d’un bas débit et d’une hypotension orthostatique. La marge de manœuvre dans cette pathologie est réduite, avec l’apparition rapide de signes congestifs en cas de non-respect du régime sans sel ou si les doses de diurétiques sont insuffisantes. De plus, les doses doivent être adaptées en fonction de l’insuffisance rénale souvent associée.
En pratique
L’IC-FSP est aujourd’hui une pathologie fréquente dont le diagnostic et la prise en charge restent à mieux définir afin d’améliorer le pronostic qui n’a pas évolué depuis 20 ans.
Son importance incite à accentuer nos efforts pour le diagnostic et la réalisation de nouvelles études randomisées afin de mieux valider le traitement.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :







