Publié le 24 oct 2006Lecture 15 min
Prothèses valvulaires percutanées : déjà demain
J.-L. MONIN, CHU Henri Mondor, Créteil
ESC et WWC
Le développement des prothèses valvulaires aortiques percutanées constitue certainement la nouveauté la plus marquante de ces trois dernières années en pathologie valvulaire. À l’instar de l’angioplastie coronaire il y a vingt ans, cette technique deviendra vraisemblablement une alternative courante au remplacement valvulaire chirurgical dans un avenir proche.
Dans la continuité, les techniques de plastie mitrale percutanée commencent à se développer et les prothèses mécaniques percutanées issues de la nanotechnologie sont déjà à l’étude. Pour le reste de cette cuvée 2006, on retiendra les registres multicentriques sur l’endocardite, l’échographie 3D-temps-réel et le scanner multicoupes pour la pathologie mitrale.
Prothèses valvulaires percutanées/plastie mitrale percutanée
Implantation percutanée de la prothèse aortique Cribier-Edwards : suivi à moyen terme
C. Tron et al [2570]
Pour la troisième année consécutive, l’équipe de Rouen a présenté les résultats de la première prothèse aortique implantable par voie percutanée, inventée par Alain Cribier et commercialisée par Edwards (figure 1). Rappelons que cette prothèse est actuellement réservée aux patients les plus graves : rétrécissement aortique en classe IV NYHA avec plusieurs comorbidités entraînant un risque opératoire > 20 %. La technique et le matériel ont évolué (2 tailles de prothèses actuellement disponibles, diminution de calibre des cathéters, transition vers une implantation rétrograde (abord artériel fémoro-iliaque) grâce à un cathéter flexible facilitant le franchissement de la crosse aortique.
Figure 1. Les deux premières bioprothèses implantables par voie percutanée, mises au point par deux équipes françaises, actuellement en cours de validation clinique.
Ce qu’il faut retenir des résultats présentés sur les 37 premiers patients implantés en France :
• le taux de succès élevé (75 %) malgré l’utilisation de la voie antérograde (transseptale, plus difficile techniquement) dans la plupart des cas,
• l’amélioration hémodynamique spectaculaire après implantation (surface valvulaire de 0,6 ± 0,1 cm2 à 1,7 ± 0,1 cm2, p < 0,0001),
• de même que l’amélioration fonctionnelle constante.
Le taux de survie relativement bas à moyen terme (37 %) s’explique en grande partie par des décès d’origine extracardiaque (essentiellement par cancer, insuffisance rénale ou sepsis), compte-tenu du terrain extrêmement défavorable des patients traités.
Remplacement valvulaire aortique percutané
Session organisée par CoreValve
La prothèse CoreValve (figure 1) est chronologiquement la deuxième bioprothèse percutanée après la Cribier-Edwards à connaître un développement clinique. Au cours de cette session, les résultats de la dernière étude clinique menée avec cette prothèse ont été présentés par C. Ruiz (New-York, USA), ainsi que plusieurs exemples cliniques par J.-C. Laborde (Toulouse, France). P. Serruys (Rotterdam, Pays-Bas) a résumé les caractéristiques et résultats actuels avec ces deux prothèses (tableau 1). Ces résultats montrent que, chez des patients à haut risque, la mortalité opératoire rapportée avec ces prothèses percutanées est réduite de moitié comparativement au risque chirurgical théorique estimé par l’EuroSCORE, avec un taux de succès d’implantation > 80 %.
En 2006, deux nouveaux essais ont débuté :
• REVIVE (Cribier-Edwards) qui doit inclure 90 patients dans 15 centres Européens,
• et COR-2006-2 (CoreValve) prévu pour 100 patients dans 12 centres en Europe et au Canada.
À noter que les critères d’inclusion de ces deux essais sont moins sévères que précédemment (profil de risque des patients moins élevé).
P. Serruys a ensuite évoqué le futur possible avec des prototypes de prothèses mécaniques issues de la nanotechnologie actuellement à l’étude (eNitinol™ Membrane, PercValve™) ; ces prothèses, extrêmement fines, pourraient être chargées sur des cathéters de 10 French pour une implantation percutanée par voie artérielle rétrograde. À voir lors des prochaines éditions de l’ESC/AHA si ces prothèses futuristes tiennent leurs promesses.
Plastie mitrale percutanée : première expérience clinique
L.-L. Rodriguez et al [P5200]
La technique d’Alfieri, adaptée pour la voie percutanée, consiste en la mise en place d’un ou deux clips sur la portion médiane des deux feuillets mitraux, créant ainsi un double orifice. L’expérience la Cleveland Clinic, dans le cadre de l’étude EVEREST 1 (Endovascular Valve Edge-to-edge REpair STudy), regroupe 12 tentatives d’implantation par voie antérograde (transseptale). Les patients inclus avaient une insuffisance mitrale de grade ≥ 3/4, d’origine dégénérative (prolapsus, n = 6) ou restrictive (cardiomyopathie, n = 6). Malgré un échec de procédure et un AVC sans séquelle, aucun décès n’est à déplorer dans cette série. Une réduction significative de l’insuffisance mitrale a été obtenue grâce à la mise en place d’un seul clip (n = 6 patients, temps moyen de procédure : 2 h 30 min) ou de 2 clips (n = 5 patients, temps moyen = 5 h pour les 3 premiers, réduit à 3 h pour les 2 derniers). Ces résultats sont donc très préliminaires et les techniques de plastie mitrale percutanée vont devoir faire la preuve de leur fiabilité et surtout de leur efficacité à long terme.
Endocardites sur prothèse ou sur valves natives
Endocardite sur prothèse ou sur pacemaker : données du registre international ICE
C.-K. Naber et al [3454]
Le registre ICE (International Collaboration on Endocarditis) regroupe 61 centres répartis dans 28 pays en Europe et aux USA. Parmi les 2 761 cas d’endocardite inclus entre janvier 2000 et août 2005, on dénombre 787 patients (29 %) ayant une prothèse valvulaire (n = 472, 17 %) ou autre matériel de type pacemaker ou défibrillateur implantable (n = 315, 12 %). L’échocardiographie a confirmé le diagnostic d’endocardite dans 88 et 93 % des cas et la chirurgie a été pratiquée en phase aiguë dans 49 et 59 % des cas d’endocardites sur prothèse ou sur pacemaker, respectivement. La répartition des germes et le taux de complications sont détaillés dans le tableau 2. À retenir la forte prévalence des endocardites à staphylocoque doré et une mortalité globale comparable dans les deux groupes, malgré un taux de complications plus élevé en cas d’endocardite sur prothèse, comparé aux autres dispositifs intracardiaques.
Complications cérébrales de l’endocardite
F. Thuny et al [3455]
Cette étude bicentrique (Marseille, hôpital de La Timone et Amiens) regroupe 385 patients avec un diagnostic établi d’endocardite sur valve native, suivis de manière prospective. Une complication cérébrale est survenue chez 85 patients au total (22 %) dont 20 complications survenues après le diagnostic d’endocardite (5 %). Les facteurs prédictifs indépendants des complications neurologiques sont la localisation mitrale et une endocardite à staphylocoque doré ; les complications cérébrales post-diagnostic sont reliées au staphylocoque doré et à la taille des végétations (> 10 mm, mesurée par ETO). La mortalité à 6 mois des complications cérébrales est de 20 % dans cette série et la chirurgie précoce (pratiquée en moyenne au 10e jour après le diagnostic) a un effet bénéfique sur la mortalité à 6 mois (6 vs 38 %, p = 0,001) en intégrant le fait que les patients non opérés avaient un score de Glasgow et un état général plus péjoratifs que les patients opérés.
Diabète et endocardite
F. Chirillo et al [3457]
Dans une série italienne de 227 patients avec diagnostic d’endocardite, parmi lesquels 28 patients diabétiques (12 %), le délai du diagnostic, la localisation valvulaire et la fréquence des abcès paravalvulaires sont comparables entre diabétiques et non- diabétiques. En revanche, la fréquence d’endocardite à staphylocoque aureus est plus élevée chez les diabétiques (36 % vs 19 %, p = 0,04) et le diabète apparaît comme un facteur de risque indépendant de décès hospitalier (39 % vs 20 %, OR = 2,49 ; IC95% : 1,10-5,62, p = 0,02) et de mortalité opératoire (OR = 4,56 ; IC95% : 1,02-20,2, p = 0,04).
Endocardite plurivalvulaire
E. Villacorta Arguelles et al [3459]
Dans une dernière série multicentrique espagnole concernant une cohorte de 574 endocardites dont 95 endocardites plurivalvulaires, une fois de plus, le staphylocoque doré est le germe le plus fréquent (23 %) et la chirurgie précoce est pratiquée dans un quart des cas (26 %), essentiellement pour insuffisance cardiaque réfractaire (79 %) ou processus infectieux non contrôlé (42 %). L’atteinte multivalvulaire est associée à un plus fort taux d’insuffisance cardiaque (64 vs 47 %, p = 0,003), d’insuffisance rénale (43 vs 33 %, p = 0,069) et de chirurgie en urgence (71 vs 52 %, p = 0,001). Cependant, la mortalité hospitalière n’est pas plus élevée en cas de localisation plurivalvulaire (32 vs 28 %, p = 0,426) ; cela s’explique probablement par le recours plus fréquent à une chirurgie précoce dans ce cas.
Insuffisance mitrale postinfarctus
Une session complète fut dédiée à l’insuffisance mitrale ischémique, prouvant que les travaux de L. Piérard et P. Lancellotti ont stimulé la recherche sur le sujet.
Insuffisance mitrale après syndrome coronaire aigu
L. Perez De Isla et al [3677]
Première étude multicentrique espagnole regroupant 300 patients (âge = 67 ± 13 ans ; 72 % d’hommes) avec un syndrome coronarien aigu (SCA) sans sus-décalage de ST. Au décours de l’épisode aigu, une insuffisance mitrale (IM) est retrouvée dans 42 % des cas (126 patients), d’importance minime à modérée pour la plupart. Après un suivi moyen d’un an, le seul facteur prédictif indépendant pour la mortalité est la présence d’une IM (RR = 5,0, IC95% : 1,03 - 24,4 ; p = 0,04). Cependant, compte-tenu de l’absence de dysfonction ventriculaire gauche (VG) sévère ou de remodelage ventriculaire, les auteurs n’expliquent pas le mécanisme de l’IM (extension de l’ischémie ?) ni par quel biais elle influence le pronostic.
Facteurs prédictifs des échecs d’annuloplastie dans l’IM ischémique
J. Mage et al [3678]
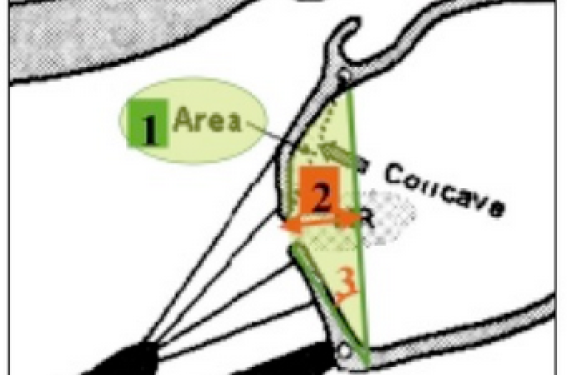
L’équipe de J.-G. Dumesnil et P. Pibarot (Saint-Foix, Canada) a mesuré la surface sous la tente (tenting area), l’angle entre feuillet mitral postérieur et plan de l’anneau et la distance coaptation/plan de l’anneau (figure 2) chez 30 patients consécutifs avant chirurgie pour IM ischémique (annuloplastie simple). Un échec de plastie, défini par une vena contracta de l’IM > 3 mm, est retrouvé dans 7 cas (23 %). Les facteurs prédictifs d’un échec de plastie sont une surface sous la tente > 2,1 cm2 (sensibilité (Ss)= 86 %, spécificité (Sp)= 91 %), une distance coaptation/anneau > 10 mm (Ss = 100 %, Sp = 78 %) et un angle entre le feuillet mitral postérieur et le plan de l’anneau > 45° (Ss = 100 %, Sp = 96%). Notons que les valeurs seuil pour la tenting area et la distance coaptation/anneau sont nettement inférieures à celles publiées par Yiu (Mayo Clinic) ou par l’équipe de Liège ; ceci est probablement lié au fait que la fonction systolique VG était peu altérée en moyenne dans cette étude. Cette série relativement courte confirme l’importance de la traction antérieure de l’appareil mitral dans la physiopathologie de l’IM ischémique et le fait que la mise en place d’un anneau sous-dimensionné ne résout qu’inconstamment ce problème.
Figure 2. Principales mesures géométriques corrélées avec le degré d'insuffisance mitrale postinfarctus : 1/surface sous la tente (tenting area) ; 2/distance coaptation/plan de l'anneau ; 3/angle entre le feuillet postérieur et le plan de l'anneau (3678).
Valeur pronostique de l’IM dynamique
Pinon et al [3679]
La valeur pronostique d’un IM d’effort a été testée chez 323 patients consécutifs ayant une dysfonction VG d’origine ischémique (fraction d’éjection < 45 %). Un point important est l’inclusion des patients ayant une ischémie myocardique à l’effort, ce qui n’était pas le cas dans les différentes séries de l’équipe de Liège. La cinétique segmentaire VG était analysée au repos et au pic de l’effort et l’IM était quantifiée au repos et dans les 30 secondes suivant l’arrêt de l’effort. Au cours d’un suivi moyen de 18 mois, 43 événements graves sont survenus (34 décès et 9 récidives d’infarctus). Les facteurs prédictifs indépendants de la mortalité d’origine cardiaque étaient l’IM au repos, le produit de la fréquence par la pression lors de l’épreuve d’effort, l’extension de l’ischémie (index de cinétique segmentaire au pic de l’effort) et l’aggravation de l’IM à l’effort. Ces résultats confirment l’importance de l’IM dynamique, dont la valeur pronostique est indépendante d’une éventuelle ischémie documentée à l’effort.
Insuffisance mitrale postinfarctus et insuffisance cardiaque
D. Aronson et al [3681]
Pour cette étude israélienne, un écho-Doppler cardiaque a été pratiqué chez 1 190 patients à 7 ± 3 jours d’un infarctus du myocarde aigu ; les patients ont été classés en trois groupes :
• absence d’IM,
• IM minime,
• IM modérée à sévère.
Une IM minime est retrouvée dans 40 % des cas, une IM modérée à sévère dans 6 % des cas. Les courbes de Kaplan-Meier (figure 3) montrent une relation significative entre la présence d’une IM et la survenue ultérieure d’une décompensation cardiaque. Le risque relatif de décompensation cardiaque est de 2,6 (IC95% : 1,6-4,1; p < 0,0001) en cas d’IM minime et de 3,6 (IC95% : 2,0-6,7; p < 0,0001) en cas d’IM modérée à sévère. Cette étude confirme le lien entre la présence d’une IM en postinfarctus et la survenue ultérieure d’une insuffisance cardiaque.
Figure 3. Courbes de Kaplan Meier : probabilité cumulée d'insuffisance cardiaque en fonction du degré d'insuffisance mitrale postinfarctus (3681).
Chirurgie valvulaire
Discongruence patient-prothèse en position mitrale
J. Magne et al [4880]
Pour ce travail franco-canadien regroupant 929 patients opérés d’un remplacement valvulaire mitral, la surface fonctionnelle de la prothèse (obtenue d’après les données d’études cliniques) divisée par la surface corporelle du patient permet de calculer la surface effective indexée (SEI). En position mitrale, une discongruence patient-prothèse (DPP) sévère est définie par une SEI < 0,9 cm²/m² ; une DPP modérée par une SEI entre 0,9 cm²/m² et 1,2 cm²/m² et l’absence de DPP lorsque la SEI est > 1,2 cm²/m². Dans cette série, une DPP modérée ou sévère était retrouvée dans 69 % et 9 % des cas respectivement. En cas de DPP sévère, la survie à 6 ans (74 ± 5 %) et 12 ans (63 ± 7%) était significativement plus basse qu’en cas de DPP modérée (84 ± 1 % et 76 ± 2 %; p = 0,027) ou absente (90 ± 2 % et 82 ± 4 %; p = 0,002). La présence d’une DPP était un facteur prédictif indépendant de mortalité à long terme (RR : 3,2 [IC95% : 1,5-6,8] ; p = 0,003). Les auteurs concluent que la DPP est un facteur indépendant de mortalité à long terme, qui peut être évité en calculant la SEI pour chaque prothèse valvulaire avant l’implantation et en choisissant le meilleur profil hémodynamique afin d’éviter une discongruence sévère.
Conséquences d’une deuxième CEC pour révision de plastie mitrale
A.-R. Raney et al [4885]
Le résultat fonctionnel d’une plastie mitrale est systématiquement évalué par une échographie transœsophagienne peropératoire, afin de rechercher une IM résiduelle, une plastie sténosante ou une obstruction dynamique intra-VG (SAM). Entre 2000 et 2005, 207 patients consécutifs ont bénéficié d’une plastie mitrale dans le centre de Newport Beach (USA). Une seconde CEC a été nécessaire chez 24 patients (12 %) pour IM résiduelle, accompagnée d’un SAM dans 8 cas (4 %). La plastie a pu être optimisée avec un bon résultat final chez 19 patients (79 % des révisions) par les procédures suivantes :
• changement de taille d’anneau (n = 10),
• ajustement de cordages en Gore-tex (n = 7),
• suture de fentes entre les différentes portions du feuillet postérieur (n = 6)
• ou plastie de glissement (n = 4).
Pour les 5 derniers patients, la valve a été remplacée. La révision a augmenté le temps de CEC de 90 min en moyenne (de 194 ± 72 min à 284 ± 69 min), sans effet délétère sur la fraction d’éjection VG évaluée à 4 mois (59 ± 9 %). Il est conclu qu’une 2e CEC permet d’optimiser les résultats d’une plastie mitrale, évitant ainsi un remplacement valvulaire dans 8 cas sur 10.
Évolution à long terme de l’intervention de Ross pratiquée à l’âge adulte
L.-L. Klieverikb et al [2572]
L’intervention de Ross (transposition du culot pulmonaire en position aortique avec homogreffe pulmonaire) donne d’excellents résultats chez l’enfant, plus controversés chez l’adulte. L’équipe d’Erasmus (Rotterdam, Pays-Bas) rapporte le suivi de 94 patients consécutifs opérés entre 1988 et 2005. L’âge moyen lors de l’intervention est de 30 ans et la durée moyenne du suivi de 9 ans. La mortalité hospitalière est de 3 % avec une survie à 10 ans de 96 ± 2 %. Cependant, 21 patients ont dû être réopérés pour dilatation progressive du néo-culot aortique, dont 5 ont dû également subir un remplacement de l’homogreffe pulmonaire. De ce fait, le taux de réopération est de 22 % à 10 ans et 40 % à 12 ans. Les auteurs concluent qu’une surveillance attentive et prolongée est nécessaire après une intervention de Ross chez l’adulte.
Plastie mitrale/rétrécissement mitral/imagerie multimodalité
Revascularisation avec ou sans plastie mitrale dans l’IM ischémique : influence de la viabilité myocardique
J.-B. Le Polain de Waroux et al [P5196]
L’équipe de J.-L. Vanoverschelde a suivi pendant 4 ans 76 patients (61 hommes d’âge moyen 62 ± 9 ans) coronariens avec dysfonction VG (fraction d’éjection 37 ± 10 %) et insuffisance mitrale au moins modérée (grade ≥ 2/4), dont 34 ont été opérés de pontages coronaires associés à une annuloplastie mitrale sous-dimensionnée (technique de Bolling) et 42 de pontages seuls. Chaque groupe était subdivisé en fonction de la présence ou de l’absence de viabilité myocardique évaluée par échographie-dobutamine préopératoire. Les quatre groupes étaient comparables au départ ; cependant la survie postopératoire (J30) était moins bonne dans le groupe pontage + plastie (83 %) que dans le groupe pontage seul (96 %, p = 0,06), indépendamment de la viabilité. La survie à 4 ans était meilleure en cas de viabilité, indépendamment de la plastie mitrale (76 ± 10 %), par comparaison aux patients sans viabilité qui avaient eu des pontages seuls (56 ± 9 %) ou pontages + plastie (35 ± 11 %, p < 0,01 vs viabilité). Concernant la mortalité à long terme dans cette population, la présence d’une viabilité avait un effet bénéfique (OR : 0,14 ; IC95% 0,05-0,38 ; p < 0,001) alors que la plastie mitrale était délétère (OR : 3,54, IC95% 1,48-8,50], p = 0,004), les deux autres facteurs prédictifs étant l’EuroSCORE et la fraction d’éjection. Il est conclu qu’en présence d’une IM postinfarctus, la survie postopératoire est influencée essentiellement par la viabilité et qu’une annuloplastie sous-dimensionnée ne modifie pas le pronostic, sauf en l’absence de viabilité où l’annuloplastie est délétère.
Rétrécissement mitral : limites du temps de demi-pression
Session FOCUS sur les cas cliniques difficiles en pathologie valvulaire
Ehud Schwammenthal (Tel Hashomer, Israël) a rappelé les limites du temps de demi-pression (pressure half time, PHT) pour l’évaluation du rétrécissement mitral. En effet, le PHT mitral ne dépend pas exclusivement de la surface valvulaire, mais également d’une éventuelle insuffisance aortique ou shunt auriculaire associé, de la compliance de l’oreillette et du ventricule gauche. L’ensemble de ces facteurs tend à diminuer le PHT, donc à surestimer la surface mitrale. Les règles d’utilisation du PHT sont donc résumées sur la figure 4, à laquelle il convient d’ajouter l’aphorisme suivant : le temps de demi-pression ne fait que la moitié du travail ; en cas de discordance, il est impératif d’avoir recours à la planimétrie 2D (méthode de référence) et/ou à l’équation de continuité ou à la zone de convergence, si elles sont applicables.
Figure 4. Limites d'utilisation du temps de demi-pression mitrale (PHT), d'après la session FOCUS "cas difficiles en pathologie valvulaire". Remerciements chaleureux au Pr Ehud Schwammenthal.
Rétrécissement mitral : évaluation de la surface mitrale par scanner multicoupes
D. Messika-Zeitoun et al [P5209]
L’évaluation de la surface mitrale par planimétrie nécessite une expertise, afin de positionner le plan de coupe à la pointe des feuillets. Le scanner multicoupes permet de sélectionner le plan de coupe adéquat à partir d’une reconstruction du volume cardiaque en trois dimensions. Chez 29 patients ayant un rétrécissement mitral en rythme sinusal, la surface mitrale mesurée par scanner (deux experts et un technicien non expert en valvulopathies) a été comparée à la surface mesurée par planimétrie (un échocardiographiste expert). Les mesures de surface mitrale obtenues par scanner en 3 ± 1 minutes (1,51 ± 0,5 cm2, [0,85 - 2,4 cm2]) étaient parfaitement corrélées aux mesures échographiques (1,4 ± 0,5 cm2, [0,7 - 2,3 cm2] ; p = 0,15 ; r = 0,88). La variabilité inter/intraobservateur était de l’ordre de 0,1 cm² et les mesures prises par le technicien non expert en valvulopathies étaient également corrélées aux mesures échographiques (1,5 ± 0,5 cm², p = 0,70, r = 0,89). Il est conclu que la surface mitrale peut être mesurée de manière fiable et non opérateur-dépendante par le scanner multicoupes, qui apparaît comme une alternative potentielle en cas de difficultés techniques en échocardiographie.
Intérêt de l’échographie 3D-temps-réel pour la surface mitrale avant et après valvuloplastie percutanée
D. Messika-Zeitoun et al [P5214]
Une deuxième étude de l’équipe d’A. Vahanian (hôpital Bichat, Paris) a évalué la fiabilité de l’échographie 3D-temps-réel (3DRT) comparée à la planimétrie (échographie 2D) effectuée par un expert. Cette série comprend 60 patients. Avant valvuloplastie mitrale percutanée (VMP), les mesures 3DRT ont tendance à surestimer la surface mitrale par rapport au 2D (1,2 ± 0,3 cm2 vs 1,1 ± 0,2 cm2 ; p = 0,0001) ; après valvuloplastie, les mesures 3DRT sont très proches des mesures 2D (1,9 ± 0,4 vs 1,9 ± 0,3 cm2, p = 0,36 ; corrélation : r = 0,76, p < 0,0001). De plus, la variabilité intra/interobservateur est faible et ne diffère pas entre un opérateur expert ou non expert en ce qui concerne le 3DRT. Enfin, le degré d’ouverture commissurale est sous-estimé par l’échographie 2D par rapport au 3DRT chez un tiers des patients. Il est conclu que l’échographie 3DRT donne une mesure fiable de la surface mitrale avant et après VMP, sans nécessité d’une expertise par opposition à l’échographie 2D ; l’ouverture des commissures semble analysée de manière plus précise en 3DRT.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :
Articles sur le même thème
publicité
publicité