Mise au point
Publié le 30 nov 2015Lecture 5 min
Diagnostic d’apnées du sommeil par prothèse rythmique implantable : et après ?
P. DEFAYE, unité de rythmologie et stimulation cardiaque, CHU de Grenoble
Le syndrome d’apnée du sommeil (SAS) est le trouble respiratoire le plus commun. Il est reconnu que 4 % des hommes et 2 % des femmes en sont affectés bien qu’une forte proportion de patients de la population générale reste non diagnostiquée, dont les porteurs de stimulateurs et défibrillateurs(1).
Le SAS est défini comme une interruption totale (apnée) ou partielle (hypopnée) du flux d’air pendant le sommeil, entraînant une diminution de la saturation du sang en oxygène et une fragmentation du sommeil.
Les apnées et les hypopnées sont appelées troubles respiratoires du sommeil ou SDB (sleep disordered breathing). En raison de sa forte prévalence, le SAS peut être à l’origine de problèmes sociaux et économiques importants ainsi que d’une augmentation de la morbidité et mortalité cardiovasculaire(2,3). Les patients souffrant d’apnée du sommeil présentent souvent une hypertension artérielle et un sur-risque de maladie coronaire. Dans l’insuffisance cardiaque, il y a souvent une association d’apnées centrales et obstructives(4).
Une forte proportion de ces patients présente des troubles du rythme associés aux apnées du sommeil, la plupart du temps une fibrillation atriale. L’étude via les mémoires du stimulateur/défibrillateur de l’association entre le suivi de l’apnée et la survenue d’arythmies est particulièrement intéressante pour évaluer et valider un traitement(5,6).
Ces patients ont aussi un risque accru d’être impliqués dans des accidents de la route, ou de voir leur vie familiale, sociale et professionnelle se dégrader(2). Pour ces raisons, un diagnostic facile et précoce de cette pathologie est nécessaire.
Quels examens pour détecter le SAS ?
La polysomnographie (PSG)
C’est l’examen de référence pour le diagnostic du SAS(6). Cependant, la lourdeur de cet examen, le manque de laboratoires du sommeil disponibles, son coût élevé rend cette méthode inadaptée pour généraliser le dépistage(6). C’est pour cela que se sont développées des méthodes alternatives afin de simplifier le diagnostic du SAS, notamment les systèmes de polygraphie (PG) ambulatoires qui peuvent être réalisés à domicile, un peu comme un Holter, et également le diagnostic par prothèse rythmique implantable.
Les stimulateurs/défibrillateurs cardiaques
Les patients porteurs de stimulateur/défibrillateur cardiaque ont une prévalence importante de SAS puisqu’environ 60 % en sont porteurs mais non diagnostiqués et non traités. Nous l’avions montré dans une étude bi-centrique entre Grenoble et Bordeaux(7). Chez ces patients, les scores cliniques comme celui d’Epworth, utilisés pour le dépistage sont, comme l’interrogatoire, souvent pris en défaut. Pourtant, le traitement par pression positive continue (PPC ou CPAP) est très efficace avec une amélioration géné ralement importante des signes cliniques, du pronostic et du risque rythmique(8). Il peut donc être utile de faire le diagnostic d’apnées du sommeil grâce à l’algorithme spécifique d’un stimulateur ou d’un défibrilllateur (fonction suivi du sommeil).
Les premiers stimulateurs à permettre le diagnostic du SAS sont les Reply et Kora de Sorin. Le stimulateur détecte automatiquement via le signal de ventilation minute (MV) (figure 1), les apnées et les réductions ventilatoires (plutôt qu’hypopnées car, pour un diagnostic d’hypopnées il y a nécessité de mesurer la saturation en oxygène). Chaque cycle de signal MV est analysé pendant la période de sommeil afin de détecter des apnées et des hypopnées. L’algorithme fournit un index de perturbation respiratoire (RDI : respiratory disturbance index) pour chaque nuit sur une durée de 6 mois.
Figure 1. Une pause respiratoire, pour le stimulateur cardiaque, est une période de 10 secondes entre 2 cycles respiratoires. Elle est caractérisée par une absence de variations significatives de l’impédance transthoracique.
Cet algorithme a été validé une première fois en 2004(9) puis amélioré et validé par l’étude DREAM publiée en 2014(10) qui a permis de valider la précision de l’algorithme en le comparant durant une même nuit à une polysomnographie réalisée au laboratoire du sommeil. Cette étude multicentrique européenne a inclus 40 patients, dont 56 % avaient un SAS sévère (IAH > 15 événements/heure de sommeil), confirmant la prévalence élevée dans cette population. Le seuil optimal défini pour la détection des patients porteurs d’un SAS sévère est un RDI calculé par le stimulateur supérieur à 20 événements par heure de sommeil.
Les avantages de la détection par prothèse
La détection de l’apnée du sommeil par une prothèse, stimulateur ou défibrillateur, a un certain nombre d’avantages. Cela permet d’intégrer le dépistage du SAS en routine, ce qui n’est pas possible avec la polysomnographie ou la polygraphie.
Ensuite, le stimulateur cardiaque fournit des données (index RDI) pour chaque nuit sur une durée de 6 mois et sans surcoût. Cet indicateur permet de suivre la compliance du patient lorsque celui-ci est traité par PPC et également d’étudier les relations entre SAS et arythmies, dont l’impact du traitement sur les arythmies (figures 2 à 5, tableau). Une anomalie significative (> 20 événements/heure) détectée par le stimulateur doit générer une confirmation diagnostique qui peut être une simple polygraphie ambulatoire. Le suivi sera ensuite partagé, en tenant compte des informations régulièrement fournies par l’appareil.
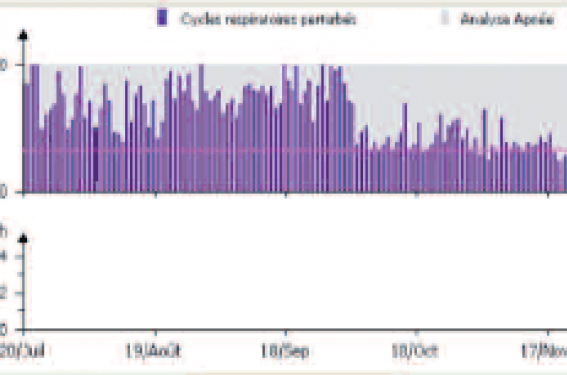
Figure 2. Patient de 80 ans implanté pour un BAV complet syncopal en février 2014, sans symptôme évocateur de SAS. Au suivi à 2 mois, il y a une forte suspicion de SAS avec 7 nuits avec RDI > 20 (RDI = 55/h de sommeil).
Figure 3. Épisodes de BAV nocturnes, en rapport avec un SAS sévère.
Figure 4. Fibrillation atriale paroxystique pendant la sieste.
Figure 5. Amélioration après traitement par PPC, avec un RDI < 20/heure de sommeil.
La détection du syndrome d’apnées du sommeil est actuellement possible avec les stimulateurs Sorin et les stimulateurs et défibrillateurs Boston Scientific (figure 6). Pour Boston Scientific, l’algorithme a été validé sur une petite série de patients par A. Shalabi(11). Deux études sont en cours, Airless, que nous coordonnons à Grenoble, et VASA en Autriche pour valider l’algorithme par rapport à la polysomnographie et évaluer les relations avec les arythmies auriculaires et ventriculaires.
Figure 6. Exemple du suivi du sommeil (événements/h) sur stimulateur et défibrillateur Boston Scientific.
Conclusion
Les algorithmes de détection de l’apnée du sommeil sont précis, validés versus la polysomnographie et permettant de dépister de façon fiable le SAS, d’autant plus que la prévalence de l’apnée est très élevée dans cette population (60 %).
Pour l’instant, en cas de RDS > 20, il faut adresser le patient pour une polygraphie de confirmation prétraitement ; si le RDS est < 15, on peut considérer que le patient n’est pas porteur d’un SAS, avec une grande fiabilité.
Le suivi à long terme permet d’évaluer de façon fiable la compliance à la PPC ainsi que son efficacité. La consultation ou le télé-suivi d’un porteur de prothèse rythmique implantable devrait toujours inclure l’étude des courbes de la fonction sommeil lorsque l’appareil implanté en dispose.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :


