Mise au point
Publié le 01 oct 2017Lecture 6 min
Fibrose de l'oreillette gauche à l'IRM et ablation de FA persistante
Fiorella SALERNO, Jérôme LACOTTE, Mina AIT SAID, Jérôme HORVILLEUR, Vladimir MANENTI, Jérôme GAROT, Institut Cardiovasculaire Paris Sud, Massy
L’ablation de la fibrillation atriale (FA) persistante reste dans notre pratique quotidienne un véritable défi avec une stratégie interventionnelle non standardisée et des taux de succès moindres que dans la FA paroxystique. L’IRM de l’oreillette gauche peut-elle être un allié dans ces procédures difficiles ?
L’IRM permet de quantifier le substrat fibrillant
La fibrose atriale identifiée chez les patients en FA est responsable d’altérations de la conduction et d’une augmentation de l’anisotropie, à l’origine de phénomènes de réentrée essentiels dans l’initiation et le maintien de la FA.
Plusieurs travaux ont montré la possibilité de visualiser cette fibrose intra-atriale par IRM, dont une étude majeure réalisée il y a 8 ans par R.S. Oakes et al. Il en ressort qu’en plus de l’analyse de l’anatomie atriale, l’IRM offre aussi par l’analyse du rehaussement tardif (RT-IRM) de l’oreillette gauche (OG), une méthode non invasive pour quantifier et localiser la fibrose structurelle, très bien corrélée au substrat fonctionnel évalué par l’étendue des zones de bas voltage en cartographie peropératoire (figure 1)(1).
Figure 1. Fibrose atriale préablation (flèches) (Photo : J. Garot, ICPS)
L’IRM permet de prédire la réponse à une ablation standardisée
En 2014, une nouvelle étude, DECAAF(2) vient appuyer l’intérêt de l’IRM en préablation en démontrant la corrélation entre fibrose et réponse à l’ablation : les patients au stade 1 (soit moins de 10 % de tissu fibreux) avant ablation ont un taux de succès de 85,8 %, de 63 % pour le stade 2 (10-20 %), de 55 % pour le stade 3 (20 à 30 %) et de 31 % seulement pour le stade 4 (plus de 30 % de tissu fibreux).
Notons que cette étude concernait essentiellement des FA paroxystiques (64 %) et qu’elle proposait une stratégie d’ablation standardisée ne ciblant le substrat extraveineux que dans 12 % des cas.
L’IRM peut aussi identifier la fibrose résiduelle après ablation. Dans DECAAF, cette fibrose résiduelle constitue un élément prédictif puissant du risque de récidive avec pour chaque pourcentage de fibrose résiduelle une augmentation de 8,2 % du risque de récurrence des symptômes.
L’IRM permet de prédire la quantité de travail « sur mesure » à réaliser pour traiter le substrat
Une autre étude réalisée dans notre centre sur des FA persistantes et paroxystiques à substrat étendu a pu démontrer que l’extension de la fibrose détectée par l’IRM dans l’oreillette gauche est corrélée à la durée et la difficulté de la procédure d’ablation ciblant le substrat électrophysiologique(3) : temps d’ablation et durée d’intervention requis pour organiser ou arrêter la fibrillation (obtenu dans 90 % des cas), sans recourir à une déconnexion des veines pulmonaires.
L’IRM présente de toute évidence un intérêt majeur pour anticiper sur la difficulté et la longueur d’une ablation dès lors qu’on s’engage sur la voie d’un traitement individualisé, ciblant le substrat extraveineux, avec le retour en rythme sinusal, voire la non-inductibilité, comme objectif : sélection de la meilleure stratégie d’ablation, optimisation du temps de salle d’intervention, prédiction d’une possible reprise pour les patients présentant le substrat le plus étendu, avec l’espoir de ne réintervenir que sur des récidives organisées.
L’IRM fait tomber les frontières entre FA paroxystique et persistante
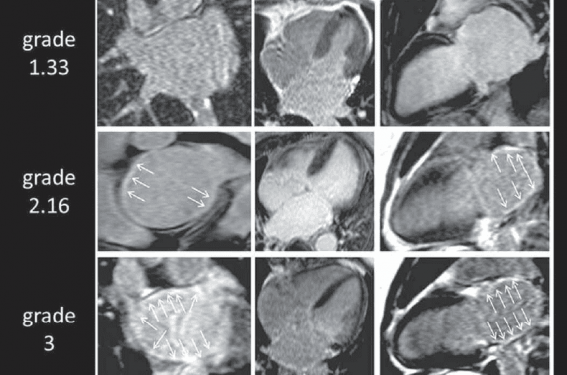
L’IRM permet donc de classer les patients en plusieurs degrés de fibrose, indépendants du type de fibrillation et des principales comorbidités et d’établir ainsi un pronostic de réponse à l’ablation, sous réserve qu’elle soit adaptée au substrat constaté. C’est ce que proposent certains auteurs(4-6), en orientant la stratégie d’ablation non plus en fonction du type de FA, paroxystique ou persistante, mais en se basant sur les stades de fibrose évalués en IRM. Ces études conduiraient à proposer un geste interventionnel préférentiellement aux stades Utah 1 et 2, pour lesquels le taux de succès apparaît plus important, écartant les patients en stade 4 (figure 2).
Figure 2. Classification Utah selon l’IRM (d’après P. Gal, N.F. Marrouche(4)).
Reste à définir comment utiliser l’IRM dans la sélection des patients et la mise en place de la meilleure stratégie d’ablation selon que l’on souhaite :
• Sélectionner un sous-groupe de patients en FA avec peu de fibrose qui sera super-répondeur à une isolation rapide et classique des veines pulmonaires.
• Identifier les patients qui nécessiteront une ablation d’emblée extensive, qu’il s’agisse de FA persistantes ou des formes paroxystiques à substrat étendu.
Au-delà du bénéfice pratique apporté par l’IRM pour prédire la difficulté et l’issue d’une 1re ablation, la question centrale reste encore l’identification peropératoire du substrat actif (driving rotors, rapid fire, etc.) et son traitement de façon consensuelle et reproductible entre opérateurs.
L’IRM va-t-elle nous aider à mieux cibler les zones à ablater dans la FA persistante ?
Indépendamment de la quantification de la fibrose atriale, la question de fond reste de définir et d’individualiser les cibles thérapeutiques ainsi que la meilleure stratégie d’ablation au plan individuel, ce qui nécessitera probablement de fusionner les données du remodelage anatomique et du substrat électrophysiologique analysé en peropératoire.
La relation CAFE versus RT-IRM a fait l’objet d’une publication par A.S. Jadidi et al.(7) en 2013 démontrant que le substrat électrophysiologique (CAFE) était topographiquement dissocié du substrat anatomique (RT-IRM), et principalement situé en périphérie des segments fibreux (figure 3). De fait, une majorité de rotors sont localisés et traités avec succès dans la zone bordante des secteurs de bas voltages, essentiellement dans les secteurs les plus hétérogènes en termes de texture fibreuse, favorables à l’anisotropie.
Si l’IRM n’a pas la résolution spatiale suffisante pour identifier précisément où se situent les cibles à traiter, elle permet au moins d’orienter la cartographie haute densité vers les secteurs les plus suspects et, dans tous les cas, d’anticiper sur la longueur et la complexité de l’ablation.
Figure 3. A : surface atriale gauche avec CAFE lors de la cartographie per ablation. B : répartition de la surface avec fibrose dense (Dense DE), hétérogène (patchy DE) ou saine (non-DE). C : répartition des zones avec CAFE entre paroi avec fibrose dense, fibrose hétérogène et paroi saine. D : proportion de surface fibrose dense/hétérogène/saine présentant des CAFE. (d’après Jadidi(7)).
Les limites de l’IRM
Trois limites restent à franchir pour démocratiser l’utilisation de l’IRM dans l’ablation de la FA :
Le manque de disponibilité machine pour une majorité de centres.
La complexité du post-traitement logiciel, puisque 15 % des IRM acquises ne sont pas exploitables par le logiciel de post-traitement(1) et que la quantification de la fibrose reste basée sur la technique de la déviation standard de la tonalité des voxels, ce qui signifie qu’il n’existe aucune mesure absolue mais seulement une estimation relative, intrinsèque à chaque patient.
La faible résolution spatiale de l’IRM, la dimension des voxels étant assez proche de l’épaisseur de la paroi atriale, explique que la segmentation 3D reste un véritable défi, difficile à automatiser et consommateur de temps.
Au cours des dernières années, l’ablation par cathétérisme de la FA a considérablement évolué. Dans le cadre de la FA persistante, la stratégie thérapeutique s’oriente de plus en plus vers une ablation « sur mesure » du substrat électrophysiologique. La question de l’apport de l’IRM dans l’amélioration des taux de succès de l’ablation par radiofréquence de la FA persistante reste posée.
Conclusion
Au quotidien, l’IRM reste pour nous un excellent outil de triage systématique avant l’ablation, en orientant les patients, paroxystiques ou persistants vers une déconnexion antrale seule ou vers une ablation extensive avec cartographie biatriale de haute densité.
Mais nos attentes vont plus loin et nous espérons que l’IRM pourra nous aider à optimiser l’ablation de la FA persistante en fusionnant les données du remodelage anatomique et du substrat électrophysiologique analysé en peropératoire.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :


