Publié le 07 oct 2012Lecture 8 min
Difficultés d’alimentation chez un nouveau-né
D. ARMENGAUD, CHI de Poissy/Saint-Germain-en-Laye
Le cas clinique que nous vous proposons ici est celui d’une petite patiente qui présente une pathologie que vous ne rencontrerez sans doute jamais !
La difficulté du diagnostic, la démarche qui a conduit à le poser, le tableau clinique, particulièrement trompeur dans un premier temps, nous ramène à la médecine… la vraie ! Celle où la réflexion et l’analyse de tous les détails sont primordiales.
Certains considéreront ce cas comme une « histoire de chasse », d’autres comme riche d’enseignement, à vous de juger.
La rédaction
Diana est une petite fille de 1 mois qui est adressée au service pédiatrie pour des difficultés d’alimentation avec une prise de poids insuffisante.
Histoire clinique
Il s’agit d’une première enfant née au terme d’une grossesse marquée par un retard de croissance intra-utérin, pour lequel une césarienne est décidée à 38 semaines d’aménorrhée et qui s’est déroulée sans problème particulier. Le poids de naissance est de 2 550 g pour une taille de 44 cm et un périmètre crânien de 34,5 cm.
Du fait de ce RCIU et de difficultés dans la prise des biberons, une sonde nasogastrique pour son alimentation est mise en place dès J3 (allaitement maternel avec complément par un lait 1er âge). Diana restera hospitalisée auprès de sa mère dans l’unité kangourou pendant 2 semaines, avec une sortie au poids de 2 830 g.
Les difficultés persistent et, à l’occasion d’une première consultation en PMI, l’enfant est réadressée dans le service en raison d’une rhinite et d’une stagnation pondérale. À l’âge de 27 jours, elle pèse 2 720 g.
L’examen clinique est cependant rassurant. Il est normal avec une enfant en bon état général, sans fièvre (37°3 C), ni gène respiratoire ni troubles hémodynamiques (FC 137/min, PA 76/49 mmHg). L’auscultation cardiopulmonaire est normale. Il n’y a pas de souffle, les pouls fémoraux sont bien perçus, la saturation de l’hémoglobine en oxygène est à 97 % en air ambiant.
Le reste de l’examen est sans particularité, notamment sur le plan digestif, chez une enfant bénéficiant d’un allaitement maternel avec un complément de lait artificiel au décours des tétées.
Le bilan biologique ne révèle pas d’anomalie notable :
• NFS :
- Hb 13,1 g/100 ml ;
- 4 290 000 GR/mm3 ; VGM : 87 µ3 ;
- 11 980 GB, avec 23 % PNN et 321 000 plaquettes.
• Ionogramme sanguin : Na : 139 ; K : 4,8 ; Cl : 105 ; RA : 23 mmol/l ; protides : 54 g/l, urée : 5,1 mmol/l ; créatinine : 34 µmol/l ;
• glycémie : 4,6 mmol/l ;– CRP : 2 mg/l.
L’interrogatoire de la mère révèle des tétées très prolongées avec une enfant qui s’endort sur le sein et ne prend que très peu de complément lacté. Des conseils diététiques sont donnés avec un retour rapide au domicile, puisque l’enfant boit correctement et prend 30 g durant les 24 heures d’observation.
La mère revient aux urgences, 4 jours plus tard, en raison de difficultés d’alimentation persistantes avec une stagnation pondérale authentifiée par une pesée à 2 850 g soit seulement 300 g de plus que son poids de naissance à presque 6 semaines de vie.
À l’examen, l’enfant présente une petite polypnée à 60/min, avec quelques signes de lutte et un freinage expiratoire sans sibilants. La saturation est à 99 % sous air ambiant. Elle est apyrétique (36°4 C) avec un temps de recoloration normal < 3 s, une auscultation cardiaque normale (FC : 150/min) et des pouls périphériques bien perçus.
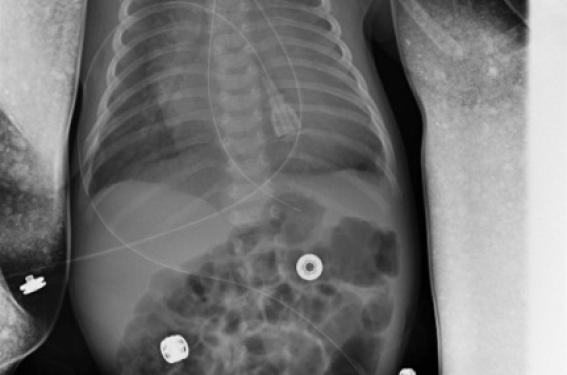
Un bilan biologique et une radiographie pulmonaire sont réalisés (figures 1 et 2).
Figure 1. Radiographie pulmonaire initiale. Pas d’anomalie du parenchyme pulmonaire (foyer ou troubles de ventilation). Doute sur une cardiomégalie ou un gros thymus.
Figure 2. 2e radiographie pulmonaire. Cardiomégalie évidente, sans troubles de ventilation.
Une sonde nasogastrique d’alimentation est mise en place, avec un apport de 8 x 60 ml en continu, accompagnée des mesures habituelles de prise en charge des bronchiolites (proclive dorsal, désobstruction rhinopharyngée et surveillance des constantes sous scope).
L’évolution est favorable en quelques jours, avec disparition de la gène respiratoire et reprise d’une courbe pondérale ascendante : prise de poids de 200 g environ en une huitaine de jours (3 010 g) faisant décider d’une reprise progressive d’une alimentation au biberon.
Mais Diana présente alors à nouveau une gêne respiratoire avec une polypnée aux alentours de 60/min et une tachycardie à 160/min au repos, régulière, sans désaturation faisant réaliser une nouvelle radiographie pulmonaire et un ECG (figure 3).
Figure 3. ECG. Tachycardie sinusale à 185/min, avec axe doit aux alentours de 60° (normal à cet âge), QT corrigé 493 ms et onde T négative en V5-V6.
L’élément préoccupant, depuis les premiers jours de vie est la difficulté à prendre du poids sans manifestations cliniques ni éléments qui pourraient orienter vers une origine digestive. Il n’y a pas de vomissements ni de diarrhée, mais une insuffisance d’apport calorique qui, du fait d’une lactation insuffisante, semble en être l’explication la plus plausible. L’anabolisme chez le nourrisson est très important et nécessite des apports de l’ordre de 100 à 110 Kcal/kg (soit 3 fois plus par kilo de poids qu’un adulte…), ce qui, compte tenu de la valeur calorique du lait de mère ou des laits « artificiels », de l’ordre de 70 Kcal/100 ml, nécessite pour cet enfant un apport de 400 à 500 ml/j. Cela rationalise la « vieille » règle d’Apert, empirique mais juste, qui est de calculer l’apport de lait nécessaire (en ml) comme le résultat de l’équation du poids (en gramme) divisé par 10 + 200.
De fait, la prise de poids est souvent correcte lorsque l’apport est réalisé par la nutrition entérale à débit constant, mais c’est le fait de téter, que ce soit au sein ou au biberon, et l’effort que cela représente qui semblent être à l’origine du problème.
Diana présentait initialement une rhinite, celle-ci a évolué banalement sans caractère obstructif ni comme des prémices d’une bronchiolite (VRS négatif). L’auscultation pulmonaire toujours normale, la normalité de la saturation de l’hémoglobine n’évoquent pas ce diagnostic. La radiographie pulmonaire ne montre ni foyer infectieux ni troubles de la ventilation.
Si le problème ne vient pas des poumons… c’est peut-être le cœur. La tachycardie est un élément en faveur d’une origine cardiaque bien qu’il n’ait pas été noté d’anomalie structurelle sur les échographies effectuées en anténatal. Cependant, il n’y a pas de souffle, ni de galop. Les pouls périphériques, et notamment fémoraux, sont bien perçus. La pression artérielle est correcte, mais la radiographie montre à l’évidence une cardiomégalie avec un index à 0,60 et un certain degré de surcharge pulmonaire traduisant une insuffisance cardiaque. L’ECG ne fait que confirmer une tachycardie régulière, sinusale, avec un PR normal, sans troubles du rythme ni de la repolarisation.
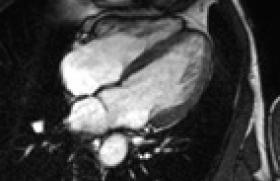
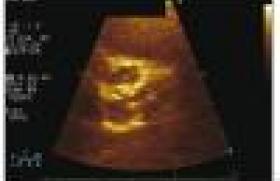
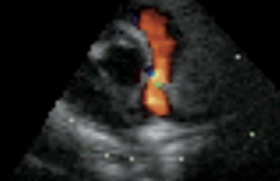
Devant la dégradation de la situation et cette insuffisance cardiaque sans étiologie décelable, l’enfant est transférée en cardiologie pour une échographie qui mettra en évidence une cardiopathie dilatée hypokinétique sans anomalie architecturale, du cœur ou des vaisseaux, ni de shunt, mais une implantation anormale de la coronaire gauche naissant de l’artère pulmonaire… L’ECG ne montre pas d’onde Q de nécrose, mais des troubles de repolarisation avec une onde T négative en D1 et en V5-V6, possiblement en rapport avec une ischémie myocardique (figure 3).
Commentaire
L’anomalie d’implantation des coronaires, principalement du fait de l’embryogenèse de la coronaire gauche à partir de l’artère pulmonaire (ALCAPA pour Anomalous origin of the Left Coronary Artery from the Pulmonary Artery ou historiquement, syndrome de Bland-White-Garland) est une pathologie « rarissime », considérée à 0,5 % de l’ensemble des cardiopathies. Elle a une incidence de 1/300 000 naissances, soit 2 à 3 cas en France par an.
Cette anomalie coronaire, isolée sans autre malformation cardiaque associée, est « silencieuse » à l’auscultation et peut se révéler par une insuffisance cardiaque rapidement progressive, comme dans ce cas, ou par un infarctus du myocarde à l’origine d’une mort subite qui survient dans 90 % des cas, non diagnostiqués dans la première année de vie.
L’ischémie myocardique du ventricule gauche est progressive du fait d’une perfusion relativement correcte en période néonatale, car la pression pulmonaire est du niveau de la pression systémique. La baisse progressive des pressions droites est à l’origine d’une baisse de perfusion de la coronaire gauche et d’ischémie myocardique, avec diminution de la contractilité du ventricule gauche, voire d’infarctus (antéro-latéral). Un réseau anastomotique peut se développer à partir de la coronaire droite limitant l’ischémie, mais pouvant aboutir à une inversion du flux de la coronaire gauche, qui se jetant « à contre-sens » dans l’artère pulmonaire, est à l’origine par ce shunt gauche-droit d’une hypervascularisation pulmonaire.
La séméiologie clinique initiale est tout à fait banale, comme dans le cas présent, avec des difficultés d’alimentation et de prise de poids. La dyspnée d’effort que représente la prise des biberons et les cris ou les pleurs douloureux pendant la prise alimentaire facilement interprétés comme une œsophagite, peuvent égarer. Une tachycardie sine materia permanente est l’élément le plus évocateur d’une origine cardiaque qui permet parfois par l’ECG (onde Q, sus-décalage de ST) de suspecter le diagnostic ou, par la pratique simple d’une radiographie du thorax, de repérer une cardiomégalie qui va conduire à la réalisation d’une échographie permettant le diagnostic (visualisation de l’anomalie d’implantation et du trajet de la coronaire gauche, inversion du flux).
L’enfant ne pourra être opérée que 3 semaines plus tard seulement en raison de la survenue de plusieurs épisodes d’ischémie myocardique aiguë nécessitant une prise en charge réanimatoire lourde du fait de l’altération profonde de la fonction du VG (index de raccourcissement des fibres effondré à 22 %). La correction de cette anomalie par la réimplantation de la coronaire sur l’aorte est pourtant réalisée et jugée comme satisfaisante, malgré la persistance d’une insuffisance ventriculaire gauche qui nécessite l’administration d’un vasodilatateur pour diminuer la postcharge en cours de récupération.
Insuffisance cardiaque du nourrisson
L’insuffisance cardiaque est l’expression de l’inaptitude du cœur à assurer un débit correspondant aux besoins. On peut y être confronté 9 fois sur 10 chez le nourrisson. Dans l’immense majorité des cas (90 %), elle est associée, ou provoquée, par une malformation cardiaque qui est le plus souvent déjà connue par la pratique des échographies anténatales.
L’insuffisance cardiaque, chez le nourrisson, est toujours droite-gauche, confondue avec une tachycardie de base ou d’effort et une cardiomégali,e traduisant l’inadaptation du myocarde à la contrainte qui lui est imposée. La diminution de la contractilité du myocarde entraîne une augmentation des pressions de remplissage aboutissant à une congestion d’amont (hépatomégalie, œdème pulmonaire) et une hypoperfusion d’aval (hypoxie et acidose tissulaire) à l’origine d’une stimulation du système rénine-angiotensine et de l’hormone antidiurétique, sources d’une rétention hydrosodée qui ne fait qu’aggraver la situation.
Il est possible de distinguer schématiquement les causes :
• causes extracardiaques
– atteinte de la volémie (déshydratation-anémie ; remplissage excessif-polyglobulie) ;
– hypertension artérielle systémique, jamais « essentielle » chez l’enfant (IRA, SHU, sténose aortique, rénale) ou pulmonaire.
• anomalies du rythme
– bradycardie (bloc auriculo-ventriculaire) ;
– tachycardie (supraventriculaire, hyperthyroïdie, shunt gauche-droite « non soufflant car extracardiaque », fistule de la veine de Galien, angiomatose hépatique, retour veineux pulmonaire anormal).
• cardiopathies congénitales (de loin les plus fréquentes)
– de diagnostic anténatal connu et s’accompagnant « toujours » d’anomalies auscultatoires, que l’on de détaillera pas ici, en rappelant leur révélation parfois retardée du fait de l’égalité de pression droite-gauche en période néonatale qui limite le débit des shunts (CIA, CIV) et de la fermeture progressive du canal artériel (syndrome de coarctation de l’aorte) ;
– trouble de la contractilité du myocarde ;
– myocardite « virale » ou surtout décompensation d’une maladie métabolique se révélant à l’occasion d’un épisode viral intercurrent ;
– ischémie myocardique (défaut d’implantation des coronaires, anévrysme [Kawasaki], sténose coronaire).
"Pédiatrie Pratique : publication avancée en ligne."
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :
Articles sur le même thème
publicité
publicité