Publié le 05 déc 2006Lecture 7 min
Conduite à tenir face à un thrombus coronaire dans les SCA
J. MONSEGU, hôpital du Val-de-Grâce, Paris
La présence d’un thrombus coronaire dans les syndromes coronaires aigus (SCA) est une situation fréquente. Elle est synonyme de facteur de gravité et le thrombus doit être pris en charge de façon pluridisciplinaire en associant la pharmacologie conventionnelle (aspirine, clopidogrel, héparine de bas poids moléculaire [HBPM]) et spécifique (anti-GPIIb/IIIa), et le traitement mécanique incluant l’angioplastie et les systèmes de thromboaspiration.
La présence d’un thrombus au décours des SCA est une situation fréquente liée aux mécanismes physiopathologiques de l’événement coronaire. S’il est le plus souvent visible sur les données de la coronarographie, il peut aussi échapper à l’imagerie conventionnelle, mais il doit néanmoins être pris en considération.
Il faut distinguer deux situations différentes :
• le SCA avec sus-décalage persistant du segment ST où le caractère occlusif du thrombus est responsable de l’événement nécessitant la restitution d’une perfusion coronaire afin de limiter la nécrose myocardique et ses conséquences ;
• le SCA sans sus-décalage de ST où la présence du thrombus s’intègre autour de la rupture de la plaque et où il va majorer le risque potentiel évolutif vers l’infarctus.
Le thrombus représente-t-il en lui-même un facteur prédictif péjoratif évolutif ?
L’analyse de grandes cohortes de patients montre que la présence d’un thrombus n’affecte pas de façon significative la mortalité hospitalière ; en revanche, sa présence est associée à une incidence statistiquement plus importante des infarctus non-Q (8,2 vs 5,2 %). Le risque d’occlusion coronaire perprocédure d’angioplastie est, lui aussi, majoré dès lors qu’un thrombus est présent avant le début de la procédure (5,9 vs 3,9 %).
Si l’on considère le critère composite hospitalier décès/infarctus/revascularisation secondaire, son incidence est plus élevée dans le groupe de patients présentant un thrombus (15,4 vs 11,2 %). Après ajustement à l’âge, à la présentation clinique, à un diabète préexistant et/ou à un antécédent de revascularisation, l’existence d’un thrombus apparaît comme un facteur prédictif indépendant de la survenue d’infarctus et de décès/infarctus pendant la phase hospitalière.
À 6 mois, le risque de décès/infarctus et d’infarctus reste majoré dans le groupe de patients présentant initialement un thrombus coronaire. Après ajustement, ce dernier reste un élément prédictif significatif de décès/infarctus ; néanmoins, après exclusion des patients présentant un thrombus dans un greffon veineux, ce risque disparaît.
De quels moyens disposons-nous ?
La pharmacologie
Les antiagrégants plaquettaires
Quelle que soit la présentation clinique du SCA, l’association d’aspirine et de clopidogrel a largement démontré son effet bénéfique.
Les résultats de l’étude CLARITY (Clopidogrel as Adjunctive ReperfusIon TherapY) montrent qu’une dose de charge préhospitalière de 300 mg améliore la reperfusion, sans effet sur le critère mortalité. On peut s’interroger sur cette dose de charge potentiellement trop faible pour obtenir un niveau d’inhibition de l’agrégation plaquettaire encore insuffisant et surtout trop tardif, ce qui amène à discuter une dose de 600 à 900 mg.
Avec une action plus rapide et plus importante, les anti-GP IIb/IIIa deviennent plus largement utilisés avec un bénéfice en termes de réduction d’événements hospitaliers, notamment concernant la mortalité et le taux de réocclusions.
Si le chef de file reste à l’heure actuelle l’abciximab, les « petites molécules » sont entrées dans l’arsenal thérapeutique singulièrement dans les SCA sans sus-décalage persistant du segment ST avec signes de gravité.
Les anticoagulants
Ils sont incontournables dans la prise en charge de ces patients ; le choix entre héparine non fractionnée et HBPM semble tourner à l’avantage de ces dernières en termes de récidive d’infarctus et de réocclusions.
Les thrombolytiques
La thrombolyse en préhospitalier a considérablement amélioré la prise en charge de l’infarctus à la phase aiguë, mais elle ne va lyser le thrombus que dans environ 60 % des cas (et ce, malgré l’utilisation de molécules récentes).
Elle expose aussi à un risque non négligeable de réinfarctus ou de réocclusions par un effet proagrégant. Elle n’a pas de place dans le SCA sans sus-décalage du segment ST, ni dès lors qu’on se trouve devant une image angiographique isolée de thrombus.
Les moyens « mécaniques »
L’angioplastie et le stenting
L’ensemble des travaux comparant la thrombolyse à l’angioplastie primaire dans la prise en charge de l’infarctus en phase aiguë est en faveur du traitement mécanique, à la fois en termes de réduction de mortalité, de récidives d’infarctus et de complications.
• La mise en place d’un stent en phase aiguë d’infarctus est largement admise de tous, sans surrisque de thrombose de l’endoprothèse.
• Le stenting direct, c’est-à-dire sans prédilatation au ballon, semble apporter un bénéfice en termes d’événements cardiovasculaires majeurs hospitaliers sans pour autant modifier le pronostic à moyen terme.
• La fragmentation du thrombus, quant à elle (obtenue par ce moyen mécanique au prix d’un effet « presse-purée »), ne peut nous satisfaire pleinement ; bien souvent, l’embolisation distale qui en découle est responsable, certes, d’un superbe résultat angiographique avec la restitution d’un flux TIMI 3, mais la reperfusion myocardique est totalement inefficace, comme en attestent la mesure du blush (rarement quantifié en dehors des études) ou, plus simplement, l’absence de normalisation du sus-décalage de ST.
• La place des endoprothèses imprégnées reste en cours d’évaluation dans cette situation thrombogène.
La thromboaspiration
De plus en plus utilisée notamment dans les thrombi situés de façon proximale, elle permet d’éviter, ou du moins de limiter, l’embolisation massive distale du thrombus.
Après aspiration du thrombus, la lésion coronaire peut être traitée classiquement par la mise en place d’une endoprothèse, mais il n’est pas exceptionnel de s’apercevoir que la lésion coronaire se limite à une simple plaque sans sténose significative, ce qui conduit parfois à une abstention thérapeutique mécanique, notamment chez l’adulte jeune (figures 1 et 2). Les travaux randomisés comparant ces systèmes de thromboaspiration à l’angioplastie conventionnelle manquent, d’où une utilisation encore « confidentielle ».
Les filtres
Sur le principe, cette technique est particulièrement séduisante. Malheureusement, elle est difficilement accessible car le positionnement du système nécessite la visualisation du lit d’aval, et, par ailleurs, elle reste réservée aux artères de gros calibre (≥ à 3 mm). En outre, il n’est pas rare que, lors du retrait du filtre, il y ait une migration embolique de matériel et la capacité du filtre reste faible, parfois saturée par l’importance du thrombus, si bien que l’outil perd alors son intérêt.
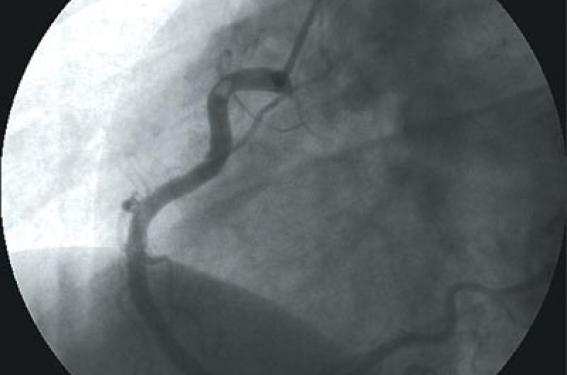
Figure 1. SCA ST- inférieur survenu au décours d’un effort chez un homme âgé de 28 ans : volumineux thrombus de la partie proximale du segment 2 de la coronaire droite.
Figure 2. Résultat après thromboaspiration sous abciximab.
Quelle stratégie retenir ?
Quelle que soit la présentation clinique du SCA, l’utilisation du triptyque aspirine–clopidogrel– HPBM est incontournable, qu’il y ait ou non présence d’un thrombus.
• Dans les SCA ST -, le thrombus est en grande partie sous-estimé par l’imagerie conventionnelle car généralement plus discret et non occlusif. Cependant, sa présence, étroitement corrélée avec les signes définissant les patients à haut risque (persistance des signes ischémiques, instabilité hémodynamique, troponinémie élevée, troubles du rythme majeurs, diabète) conduit à une attitude pharmacologique active avec l’utilisation des anti-GPIIb/IIIa dès la prise en charge ou perprocédure d’angioplastie.
• À la phase aiguë du SCA ST +, la reperfusion coronaire reste le seul but à atteindre dans un délai le plus bref possible. Si le choix entre la thrombolyse et l’angioplastie primaire échappe un peu à l’objet du propos de cet article, devant intégrer le critère temps mais aussi la disponibilité réelle d’une salle de cardiologie interventionnelle, le thrombus reste bien au centre du problème. Lorsqu’il est volumineux et très proximal sur un vaisseau de gros calibre, une thromboaspiration mérite d’être proposée avant l’angioplastie.
Mais, plutôt que d’opposer les deux alternatives de la reperfusion, est né le concept récent de l’angioplastie facilitée où une préparation pharmacologique spécifique va permettre d’aider le travail « mécanique » de l’angioplastie (figures 3, 4 et 5). Si l’étude ASSENT 4 (ASsessment of the Safety and Efficacy of a New Thrombolytic agent) semble répondre négativement concernant l’utilisation d’un thrombolytique en amont du geste, avec la réserve du moment de l’angioplastie, la métaanalyse de De Luca montre un effet bénéfique de l’abciximab administré en amont de l’angioplastie. D’autres travaux, dont l’étude FINESSE (Study of abciximab, reteplase, and heparin during acute cardiac intervention), devraient permettre de préciser l’utilisation optimale des différentes options thérapeutiques (thrombolyse, anti-GPIIb/IIIa) dont nous disposons.
Figure 3. SCA ST + antéro-septo-apical vu précocement à H2 proposé pour angioplastie primaire sous abciximab, avec occlusion de l’IVA moyenne.
Figure 4. Résultat après implantation d’une endoprothèse nue. Restitution d’un flux TIMI 3 dans l’IVA mais persistance d’une image de thrombus prédominant dans la diagonale.
Figure 5. Contrôle à J5 après poursuite des anti-GPIIb/IIIa pendant 24 heures et de l’héparinothérapie non fractionnée : disparition complète des images de thrombus.
Un autre concept mérite aussi d’être mentionné : celui de l’attentisme. Ainsi, la persistance d’une image de thrombus localisé, associée à une reperfusion coronaire avec un flux TIMI 3 et une régression du sus-décalage, doit conduire à savoir arrêter la procédure interventionnelle et poursuivre une thérapeutique anticoagulante et antiagrégante optimisée permettant un « nettoyage » de l’artère en quelques jours sans surrisque thrombotique le plus souvent.
En pratique
Le thrombus, acteur de premier rang dans les SCA, doit faire l’objet d’une prise en charge à la fois pharmacologique et mécanique, dans une stratégie qui mérite encore d’être précisée au vu des progrès technologiques et des résultats de travaux en cours.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :
Articles sur le même thème
publicité
publicité






