Vasculaire
Publié le 31 aoû 2014Lecture 15 min
Dissections aortiques - Les endoprothèses modifient la donne
J.-P. BECQUEMIN, Service de chirurgie vasculaire et thoracique et endocrinienne, Groupe hospitalier Henri Mondor, Créteil
Les dissections de l’aorte constituent un événement gravissime menaçant la vie. Le pronostic dépend essentiellement de la localisation de la porte d‘entrée et de l’existence ou non de complications. Le remplacement chirurgical de l’aorte ascendante reste le traitement habituel pour la majorité des dissections aiguës de type A, le traitement endovasculaire a désormais pris une place dans le traitement des dissections de type B et des complications. La localisation de la ou des déchirures intimales et l’analyse des flux dans le vrai et le faux chenal sont des éléments importants pour la stratégie thérapeutique. Les progrès considérables de l’imagerie permettent une meilleure compréhension de cette pathologie et ouvrent la voie aux traitements endovasculaires et à une amélioration du pronostic.
Une dissection est la conséquence d’une déchirure généralement transversale de la couche intimale, créant ainsi un plan de clivage entre intima et média dans lequel le flux sanguin circule, constituant un faux chenal. La dissection peut être antérograde, rétrograde ou mixte (figure 1). Longtemps on a pensé qu’il y avait une seule porte d’entrée et porte de sortie. En réalité, les déchirures sont souvent multiples. L’analyse des angio-scanners de 72 dissections de type B a montré qu’il y a en moyenne 2,8 ± 2,11 déchirures dans l’aorte, que ces déchirures sont situées entre 6 mm avant et 459,2 mm après l’orifice de la sous-clavière gauche, et siègent dans 80,5 % des cas en amont de tronc cœliaque. La surface de chaque déchirure est en moyenne de 0,63 cm2. Plus la surface est large, plus le faux chenal est important et plus élevé est le risque de malperfusion(1).
Pour être efficace, le traitement endovasculaire impose au préalable une imagerie de qualité pour comprendre l’anatomie et l’hémodynamique des flux de la dissection et pour planifier l’intervention.
Figure 1. Dissection mixte, antérograde et rétrograde à partir de la sous-clavière gauche (vue postérieure).
Quelle imagerie ?
Échographie
L’écho transthoracique a un intérêt indiscutable pour l’évaluation en urgence de l’aorte ascendante des valves aortiques et d’un éventuel épanchement péricardique. En per-opératoire, l’écho transœsophagienne identifie les localisations du vrai et du faux chenal, les flux, la situation des guides, la progression des endoprothèses et leur efficacité. En confrontant la position de la sonde, visualisée sur l’écran de l’appareil radio (figure 2), et l’aspect de l’aorte sur la console d‘échographie, on identifie très précisément les lésions, éléments essentiels pour la réussite du traitement.
Figure 2. Angiographie peropératoire. A. Dissection aortique et sonde d’échographie transœsophagienne. B. Résultat après mise en place de l’endoprothèse.
IRM
Elle a peu de place en urgence, du fait de sa faible disponibilité et d’une moindre résolution anatomique que le scanner, mais peut être utile à la surveillance des dissections chroniques notamment pour l’étude des flux. En postopératoire d’une endoprothèse, elle ne peut être utilisée, comme alternative au scanner, que si l’armature de celle-ci est en nitinol, et non en acier.
Angiographie par tomodensitométrie (angio-TDM)
L’exploration de l’aorte nécessite une précision que seuls les TDM multidétecteurs (TDMMB) > 16 barrettes sont capables de réaliser : acquisition d’un large volume – de la crosse de l’aorte jusqu’aux artères fémorales en un seul champ –, haute résolution spatiale, dans un temps suffisamment rapide pour obtenir une opacification vasculaire optimale après une seule injection de produit de contraste iodé. L’analyse des images de l’angio-TDM et des reconstructions en 2D et 3D est effectuée grâce aux consoles de traitement informatique (figures 3 à 5). L’interprétation des images doit être dynamique et interactive à partir des images natives : les reconstructions 3D en rendu de volume (VRT) ou en MIP avec suppression des structures osseuses peuvent être obtenues en quelques secondes. Des reconstructions additionnelles 2D multiplanaires obliques ou courbes selon l’axe central du vaisseau facilitent l’extraction de paramètres biométriques tels que le diamètre, la surface ou la longueur du vaisseau. Au besoin on peut réaliser une reconstruction endovasculaire qui visualise en 3D et en dynamique la porte d’entrée. L’angio-TDM identifie la ou les porte(s) d’entrée, le vrai et le faux chenal, l’extension de la dissection sur l’aorte et les collatérales importantes, le retentissement parenchymateux (zone ischémique rénale, hépatique, digestive) et la présence d’un hémothorax d’un hémopéritoine ou d’une simple suffusion péri-aortique. Enfin elle permet les mesures indispensables au choix de l’endoprothèse : diamètres, longueurs, proximité des zones sensibles (valves aortiques, troncs supraaortiques, artères viscérales). Elle permet également d’anticiper d’éventuels problèmes lors de la fermeture de la porte d’entrée, notamment l’occlusion de collatérales importantes.
Figure 3. Angiographie par tomodensitométrie en rendu volumique d’une dissection aiguë sans dilatation majeure de l’aorte au niveau thoracique.
Figure 4. Angiographie par tomodensitométrie avec reconstruction en 3D montrant une dissection de type B avec un volumineux faux chenal.
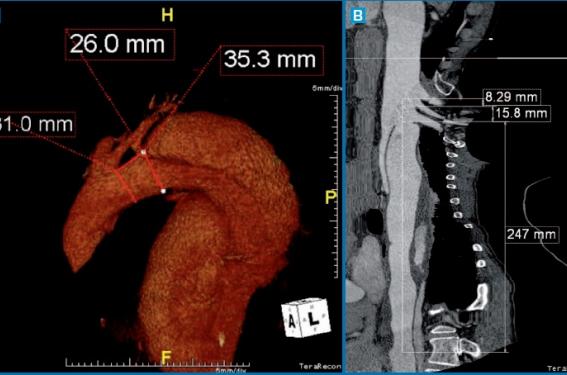
Figure 5. Angiographie par tomodensitométrie d’une dissection aortique. A. Reconstruction endovasculaire montrant la porte d’entrée de la dissection et la situation par rapport à la naissance des troncs supra-aortiques. B. Mesure des dimensions (diamètres et longueurs) de l’endoprothèse par la technique de la ligne centrale (reconstruction multiplanaire).
Quel pronostic ?
Selon le siège de la porte d’entrée, le pronostic est différent. Les dissections qui siègent en amont de la sous-clavière gauche, dites de type A dans la classification de Stanford, sont rapidement mortelles en particulier en cas de désinsertion de la valve aortique, d’un hémopéricarde, ou d’une dissection des coronaires. Le traitement chirurgical d’urgence qui assure le remplacement de l’aorte ascendante représente la meilleure chance de survie.
Pour les dissections en aval de la sous-clavière gauche dite de type B, le pronostic dépend essentiellement de la présence d’une complication. Pour les dissections de type B non compliquées, le traitement médical offre à court et moyen terme des résultats supérieurs au remplacement chirurgical de l’aorte descendante. La survie à 5 ans reste cependant inférieure à celle de la population indemne, en raison de récidives de la dissection ou de la formation d’un anévrisme, événements survenant dans près de 40 % des cas. Les dissections aiguës compliquées concernent environ 20 % des patients présentant une dissection de type B. Elles sont définies par la présence :
- d’ischémie viscérale ou des membres inférieurs ;
- de rupture ou de pré-rupture ;
- d’extension de la dissection.
La mortalité est majeure, de l‘ordre de 30 à 40 %. Contrairement aux dissections de type A, le traitement chirurgical traditionnel des dissections aiguës de type B est une entreprise majeure dont les résultats sont très décevants.
Passé la phase aiguë, qu’il s’agisse d’une dissection de type A traitée ou d’une dissection de type B, l’évolution de l’aorte non traitée peut être péjorative. De nouvelles dissections peuvent se produire (figure 6), avec les mêmes risques immédiats de rupture ou de malperfusion, et des dilatations progressives de l’aorte et/ou des iliaques, avec transformation anévrysmale (figure 7). Ces évolutions doivent être détectées par un suivi régulier par imagerie scanner ou par IRM, afin de les traiter au besoin.
Figure 6. Évolution d’une dissection de type B connue. Constitution d’une nouvelle dissection avec apparition d’un troisième chenal au scanner de suivi.
Figure 7. Extension d’un processus de dissection au carrefour aortique et aux iliaques (droite alimentée par le faux chenal, gauche par le vrai chenal), exposant à une occlusion artérielle ou à une évolution anévrismale.
Dans le groupe de patients non opérés, les données récentes (non publiées) de l’étude randomisée INSTEAD montrent qu’à long terme les patients qui ont été traités par endoprothèse ont moins de complications évolutives.
Quel traitement endovasculaire ?
Traitement des complications ischémiques
Fenestration endovasculaire
La fenestration peut être indiquée dans les dissections aiguës en cas de malperfusion(2). On place un guide dans le vrai chenal et un guide dans le faux chenal, avant de perforer le flap à l’aide d’une aiguille ou d’un cathéter de réentrée (Outback, Cordis). On peut aussi monter sur les deux guides un introducteur armé pour déchirer le flap intimal jusque dans l’aorte terminale.
Stents nus
La mise en place de stents non couverts dans les artères viscérales ou dans les iliaques permet de résoudre en urgence des syndromes de malperfusion et de limiter le temps d’ischémie des organes cibles (figure 8) au prix d’une agression minime. Cependant, le problème de la dissection aortique n’est pas réglé. En pratique, il s’agit d’un complément à la mise en place d’une endoprothèse thoracique.
Figure 8. Angioscanner avant et après mise en place d’un stent nu dans l’artère rénale pour traiter un flap obstructif de l’artère rénale.
Endoprothèses thoraciques
Principes et contraintes
Le principe consiste à introduire par voie fémorale une endoprothèse étanche qui couvre la porte d’entrée et provoque une décompression du faux chenal et sa thrombose (figure 9). La faisabilité de cette technique est établie, mais il reste de nombreuses questions non résolues. Les endoprothèses ont surtout été développées pour les anévrismes et les ruptures traumatiques isthmiques. La problématique en cas de dissection est double :
- pour les dissections aiguës, le problème majeur est la fragilité de la paroi aortique qui pourrait être accrue : par les contraintes mécaniques liées au squelette métallique de l’endoprothèse ou par la présence, pour certaines endoprothèses, de crochets latéraux visant à fixer la prothèse et prévenir sa migration. Une nouvelle endoprothèse est actuellement en cours d’évaluation (figure 10). Elle comporte deux composants, une endoprothèse couverte pour fermer la porte d’entrée proximale et un stent nu, suffisamment souples pour être correctement déployées dans les segments sinueux de l’aorte, avec un ancrage suffisant pour ne pas migrer sans être traumatisant pour la paroi, et enfin assez flexible pour s’adapter aux incongruences des zones d’apposition proximale et distale. Le principe est de fermer la porte d’entrée proximale et de plaquer le flap intimal sur la paroi aortique résiduelle. À noter qu’un autre stent est en développement pour les dissections de type A considérées comme non opérables (figure 11) ;
- pour les dissections chroniques, c’est au contraire la résistance du flap intimal fibrosé qui peut empêcher l’endoprothèse de s’expandre correctement (figure 12). Les endoprothèses actuelles peuvent être utilisées, comme pour les anévrismes athéroscléreux.
Figure 9. Traitement d’une dissection compliquée d’hémothorax (A) par endoprothèse couverte (B).
Figure 10. Endoprothèse « Cook dissection ».
Figure 11. Dissection traitée par endoprothèse couverte au niveau de la crosse et de la portion initiale de l’aorte descendante, associée à une endoprothèse non couverte « Cook dissection » dans l’aorte descendante jusqu’au diaphragme.
On connaît maintenant, grâce aux suivis par scanner, l’évolution des dissections traitées par endoprothèses. Dans le segment d’aorte couverte par l’endoprothèse, l’occlusion du faux chenal est obtenue dans la majorité des cas. En aval, la dissection persiste mais semble moins évolutive, probablement par réduction de la pression dans le faux chenal (figure 12).
Figure 12. Expansion incomplète de l’endoprothèse qui est comprimée par le faux chenal.
Des évolutions négatives ont été rapportées après mise en place d’une endoprothèse pour dissection. C’est ainsi que des dissections rétrogrades depuis la partie proximale du stent, placé au voisinage de la sous-clavière, ont été rapportées (figure 13). Elles peuvent amener à réaliser secondairement une chirurgie de l’aorte ascendante. La fermeture du faux chenal peut compromettre la vascularisation des artères viscérales lorsqu’elles naissent de celui-ci. Il convient d’anticiper ce phénomène et de perforer la fausse membrane en regard des artères concernées pour maintenir leur perméabilité par mise en place d’un stent depuis le vrai chenal.
Figure 13. Dissection rétrograde après traitement d’un anévrisme de la crosse par « débranching » des troncs supra aortiques et endoprothèse couverte : le flap s’arrête au-dessus de l’artère coronaire.
Résultats
Pour les dissections de type A, seuls quelques cas anecdotiques ont été traités. Mais sur le plan théorique l’examen des scanners de dissections de type A opérées a montré que près de 50 % des cas auraient pu être traités par endoprothèse, car l’orifice d’entrée était à distance de l’anneau aortique et des coronaires et du tronc artériel brachio-céphalique en aval. Le bon résultat de la chirurgie n’autorise pas cependant l’application large de cette technologie, mais cette option peut être proposée chez des malades considérés comme inopérables.
Pour les dissections de type B : en période aiguë (15 jours), l’étude ABSORB, qui est une étude ouverte non comparative, montre des résultats favorables.
Pour les dissections compliquées : dans le cadre des dissections subaiguës (> 15 jours) de type B non compliquées, l’étude randomisée INSTEAD comparant le traitement médical seul et le traitement médical associé à une endoprothèse n’a pas montré d’amélioration de survie à 2 ans, mais un meilleur remodelage de l’aorte traitée et une diminution du nombre d’interventions secondaires. Les résultats à 5 ans montrent un meilleur pronostic vital.
Quelles perspectives ?
Au fur et à mesure du développement des techniques endovasculaires, leur application à des cas de plus en plus complexes amène à proposer des solutions originales dont nous donnerons quelques exemples.
Dissection de type A, avec extension distale
De plus en plus souvent, on combine les techniques ouvertes et endovasculaires, on parle d’interventions hybrides.
Trompe d’éléphant proximale/endoprothèse distale
L’intervention, dérivée de l’intervention de Borst, consiste comme dans la description princeps, à remplacer par sternotomie, sous CEC et arrêt circulatoire, l’aorte ascendante et horizontale et à laisser dans l’aorte descendante un segment prothétique endoluminal. La variante proposée remplace le second temps de chirurgie ouverte par la mise en place, depuis l’artère fémorale, d’une endoprothèse thoracique dans le segment prothétique flottant. La lourdeur du deuxième temps opératoire en est considérablement allégée (figure 14).
Technique de la trompe d’éléphant « gelée » (frozen éléphant trunk)
Cette technique fait appel aux prothèses hybrides (E-vita Open, JOTEC GmbH, Hechingen), associant un segment proximal en Dacron et un segment distal comportant une endoprothèse couverte. Comme pour la technique de la trompe d’éléphant conventionnelle, le segment pathologique de la crosse aortique est réséqué sous arrêt circulatoire jusqu’à l’isthme aortique. L’endoprothèse couverte est introduite et larguée par voie antérograde dans l’aorte thoracique descendante en s’aidant d’un guide préalablement introduit par voie fémorale. L’extrémité proximale est suturée à l’isthme aortique et la prothèse tubulaire en Dacron est utilisée pour remplacer la crosse aortique avec réimplantation en palette des troncs supra-aortiques (figure 15). Les résultats de cette technique encore récente permettent d’estimer la mortalité hospitalière à 7 % et l’incidence de paraplégie postopératoire à 3 %(3).
Figure 14. Technique de la trompe d’éléphant. Dans un premier temps (à gauche) un remplacement chirurgical de la crosse est associé à la mise en place d’une prothèse suturée à l’isthme dans le vrai chenal au niveau de l’aorte descendante. Le deuxième temps (à droite) consiste à prolonger la prothèse par une endoprothèse couverte introduite par voie fémorale.
Figure 15. Prothèse Open-Evita Gamida. A. La partie proximale comporte un Dacron standard pour remplacer l’aorte ascendante ou la partie proximale de l’aorte horizontale et la partie distale est une endoprothèse qui est glissée depuis l’artériotomie proximale dans l’aorte descendante. B. Contrôle angio-TDM postopératoire.
Dissection de type B
La porte d’entrée de la dissection est souvent très proche de la sous-clavière gauche, ce qui peut nécessiter le déroutage d’un ou de plusieurs troncs supra-aortiques. En effet, la complexité de l’anatomie de la crosse limite pour l’instant une solution endovasculaire pure (nécessitant des endoprothèses fenêtrées) à quelques cas anecdotiques. Il est bien sûr obligatoire de préserver les troncs supra-aortiques, ce qui peut être réalisé par une chirurgie de déroutage de ces derniers. En fonction de l’étendue des lésions, et plus particulièrement de l’extension proximale, plusieurs procédés sont possibles. Très schématiquement, si la distance entre le tronc artériel brachio-céphalique et la carotide gauche est suffisante, les déroutages se font par voie cervicale. Lorsque cette distance est insuffisante, une sternotomie est nécessaire.
Revascularisation chirurgicale des troncs supra-aortiques
Pour la sous-clavière gauche, on a le choix entre une réimplantation de la sous-clavière dans la carotide primitive ou un pontage carotido-sous-clavier. Dans le même temps ou secondairement, la sous-clavière proximale doit être occluse pour éviter une endofuite de type II dans la crosse de l’aorte. Pour ce faire, le plus simple est de monter par voie humérale gauche un système d’occlusion (Amplatzer) qui sera largué dans la sous-clavière prévertébrale au ras de la crosse.
En cas de couverture de la carotide primitive gauche et de la sous-clavière gauche, on réalise par voie sus-claviculaire un pontage à partir de la carotide primitive droite, soit vers la sous-clavière gauche avec réimplantation de la carotide primitive gauche dans le pontage, soit vers la carotide gauche et en réimplantant la sous-clavière dans le pontage.
Enfin lorsqu’on prévoit une couverture du tronc artériel brachio-céphalique (TABC), la revascularisation est effectuée à partir de l’aorte ascendante abordée par sternotomie. Cette intervention n’est pas à recommander dans les dissections aiguës, mais elle est possible dans les dissections chroniques de type B ou chez les malades qui ont déjà eu un remplacement de l’aorte ascendante pour dissection de type A et dont le segment en aval de la réparation évolue.
Technique dite « Chymney technique »
Elle consiste à mettre en parallèle une endoprothèse aortique et une (ou plusieurs) endoprothèses dans le TABC après déroutage des troncs supra-aortiques (figure 16). Cette technique complexe n’est pas toujours efficace : elle est donc réservée aux patients à haut risque pour lesquels aucune autre possibilité technique n’est utilisable(4).
Prothèses fenêtrées et branchées
On peut maintenant proposer la réparation endovasculaire de lésions aortiques englobant l’arche, la limite étant la proximité de l’anneau aortique et le diamètre et l’état de l’aorte ascendante. Outre les problèmes technologiques (les prothèses sont fabriquées sur mesure), il y a de nombreuses difficultés techniques liées au placement de branches latérales dans un segment aortique courbe avec un trajet oblique dans les 2 plans, aux angulations fréquentes qui nuisent à la précision de déploiement, enfin à la présence de thrombus pariétal et de calcifications qui expliquent le risque d’embolie cérébrale lors des manœuvres endovasculaires.
Des essais in vitro et sur l’animal ont tenté de valider la fenestration in situ : après déploiement de l’endoprothèse dans la crosse, des cathéters sont placés depuis les carotides au contact de l’endoprothèse qui est perforée à l’aide de divers instruments (aiguilles, laser) ; le cathéter est ensuite poussé sur guide dans la lumière de l’endoprothèse, et un cutting balloon permet d’élargir l’orifice afin de mettre en place un stent couvert.
Figure 16. Reconstruction 3D postopératoire d’un malade opéré par la technique dite « Chimney » : un stent couvert a été placé dans le TABC et une endoprothèse dans la crosse de l’aorte. Auparavant les troncs supra-aortiques ont été dérivés depuis la carotide primitive droite.
Aorte thoracoabdominale
Endoprothèses fenêtrées et/ou branchées
Il est possible dans certains cas de mettre en place des endoprothèses fenêtrées ou branchées dans les dissections évolutives. Il s’agit de couvrir l’aorte viscérale en préservant la perméabilité des artères viscérales à l’aide de stents couverts (figure 17).
Techniques hybrides
Elles consistent à dérouter les branches viscérales depuis l’aorte sous-rénale ou les iliaques, avant d’implanter une endoprothèse dans l’aorte. Les résultats sont plutôt décevants et on réserve cette solution aux cas où aucune autre solution ne soit techniquement réalisable.
Figure 17. Traitement endovasculaire d’une dissection de type B traitée par une endoprothèse proximale. A. Reconstructions 3D postopératoires d’une patiente traitée pour une dissection type B de l’aorte. Dans un premier temps la porte d’entrée a été traitée à l’étage thoracique. Cette dernière s’est incomplètement ouverte. B. Reconstructions 3D postopératoires après implantation dans un deuxième temps d’une prothèse fenêtrée au niveau de l’aorte viscérale.
En pratique
Les possibilités thérapeutiques pour les dissections de l’aorte se sont considérablement étendues ces dernières années : elles permettent d’envisager une amélioration du pronostic de cette affection redoutable.
Une collaboration multidisciplinaire incluant chirurgiens vasculaires, chirurgiens cardiaques et radiologues interventionnels, et un plateau technique moderne avec des salles d’opération équipées d’une imagerie performante sont indispensables.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :