Cardiologie interventionnelle
Publié le 22 juin 2004Lecture 7 min
Le monde très actif… des stents actifs
O. VARENNE et C. SPAULDING, hôpital Cochin, Paris

Depuis la présentation des résultats de l’étude RAVEL utilisant le stent actif au sirolimus Cypher™ et ceux des études TAXUS utilisant les stents au paclitaxel Taxus™, de nombreux programmes de recherche clinique ont été élaborés.
Une des améliorations décisives des stents actifs concerne la plate-forme qui doit idéalement être la plus proche possible des stents de dernière génération.
Outre les perfectionnements attendus des stents SelectTM (Cordis) et des stents Liberte® (Boston), les deux programmes actuellement les plus avancés concernent les stents Medtronic (EndeavorTM) et les stents Guidant (ChampionTM).
Stent Endeavor™ (Medtronic)
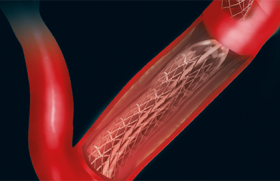
Le stent EndeavorTM (Medtronic) dérive du stent DriverTM (Medtronic), constitué d’un alliage cobalt-chrome qui permet la réalisation de mailles de seulement 0,0036” ; il est donc doté d’un meilleur profil, responsable d’une grande flexibilité, et d’une meilleure délivrabilité (figure 1).
Figure 1. Le stent EndeavorTM dérive du stent DriverTM constitué d’un alliage cobalt-chrome, de mailles de 0,0036’’ et d’une grande flexibilité et délivrabilité (Medtronic).
Le stent EndeavorTM libère dans la paroi vasculaire un composé analogue à la rapamycine, l’ABT-578. L’ABT-578 a de puissantes propriétés antiprolifératives par le blocage du récepteur TOR (affecté également par la rapamycine), entraînant une inhibition du cycle et de la prolifération cellulaires. Le polymère appliqué sur le stent DriverTM pour réaliser le stent EndeavorTM est de la phosphorylcholine qui contient 10 µg/mm3 d’ABT-578, principalement sur la face abluminale de la plate-forme.
Ce stent a été évalué dans l’étude ENDEAVOR I, qui est un registre prospectif incluant 100 patients angineux traités par stent actif EndeavorTM. Les lésions de novo devaient mesurer moins de 15 mm de longueur dans des vaisseaux de 3,0 à 3,5 mm. Le taux de succès des procédures a été de 100 %. Le taux de complications cardio-vasculaires n’a été que de 1 % pour le stent EndeavorTM à 30 jours, et de 2 % après 4 mois (1 infarctus non Q sur thrombose subaiguë en aval du stent et une revascularisation 4 mois après la procédure initiale). La perte de gain en angiographie a été de 0,33 mm (et seulement 0,20 mm dans le segment traité). Le pourcentage de sténoses a été réduit de 70,3 % en préprocédure à 5,4 % en postprocédure et 14,4 % à 4 mois. Quatre-vingt-quinze patients ont bénéficié d’une exploration par ultrasons endocoronaires, sans mise en évidence de malapposition tardive. Le volume de formation néo-intimale à 4 mois est de 0,32 ± 0,40 mm3/mm, et le pourcentage d’obstruction de la lumière de seulement 4,4 %.
Ces résultats indiquent que le stent EndeavorTM s’accompagne d’une formation limitée de néo-intima après implantation coronaire, sans effets secondaires défavorables.
Suite du programme Endeavor. Ces résultats appelaient une confirmation clinique dans un essai de grande ampleur randomisé : c’est le but de l’étude ENDEAVOR II qui a inclus 1 200 patients en 2003. Cette étude randomisée en double aveugle évalue la sécurité d’emploi et l’efficacité du stent EndeavorTM comparativement au stent DriverTM.
Les résultats préliminaires à 30 jours de l’étude ENDEAVOR II ont été présentés lors du PCR en mai dernier. Cette étude randomisée en double aveugle, a inclus 1 191 patients avec lésion de novo (2,25-3,5 mm de diamètre et 14 à 27 mm de longueur) entre l’implantation d’un stent nu DriverTM et le stent actif EndeavorTM. Le critère principal de l’étude est le taux de TVF (target vessel failure) associant décès, infarctus et revascularisation du vaisseau cible à 9 mois. Certains des patients sont inclus dans une sous-étude angiographique et échographique endocoronaire. Les lésions de type B2 et C représentent environ 75 % des lésions dans les deux groupes. Les données présentées à 30 jours retrouvent un taux d’événements cardio-vasculaires identique dans les deux groupes (2,9 % vs 3,5 %, p = ns) et un taux de thromboses de stents de 0,7 % et 1 % (p = ns). Les résultats d’efficacité seront communiqués en 2005.
Enfin, l’étude ENDEAVOR III, comparant l’efficacité du stent EndeavorTM à celle du stent CypherTM, devrait prochainement amener un élément de comparaison entre les diverses plate-formes.
Stent Champion™ (Guidant)
La plate-forme cellulaire du stent de Guidant a également été utilisée dans le cadre des études FUTURE I et II.
Les stents ChampionTM ont un bas profil (0,042”) et des mailles fines (0,0046”) leur permettant une bonne délivrabilité. Ils sont recouverts de polymère biorésorbable qui libère progressivement l’éverolimus (développé en partenariat avec Novartis), une molécule antiproliférative (dont les études expérimentales ont montré une plus grande sélectivité sur les cellules musculaires lisses que sur les cellules endothéliales) et anti-inflammatoire (figure 2).
Ce stent a été utilisé dans les études FUTURE I et II visant à valider la sécurité et l’efficacité de cette stratégie.
Figure 2. Les stents ChampionTM ont un bas profil (0,0046’’). Ils sont recouverts de polymère biorésorbable qui libère progressivement l’éverolimus, substance antiproliférative et anti-inflammatoire (Guidant).
FUTURE I a inclus 27 patients non diabétiques présentant une lésion < 18 mm dans des artères de 2,75 à 4,0 mm, randomisés entre des stents actifs ChampionTM et des stents standard. Le stent ChampionTM permet une faible perte de gain à 6 mois de 0,11 mm (versus 0,85 mm) et un volume de néo-intima obstruant la lumière intrastent de seulement 2,9 % (versus 22,4 %) ; ces résultats sont comparables à ceux des stents actifs au sirolimus et au paclitaxel validés dans des études de grande taille.
L’étude FUTURE II, voisine de la précédente, a inclus 64 patients (diabétiques autorisés) présentant des lésions identiques à celles de FUTURE I et dont 21 ont reçu un stent actif ChampionTM. Après 6 mois, la perte de gain est de 0,12 mm (versus 0,85 mm) et le volume de néo-intima en échographie endocoronaire de 1,1 % (vs 22,6 %), soit une réduction de 95 %.
Suite du programme. Ces résultats positifs et rassurants en termes de sécurité jusqu’à un an doivent bien évidemment être confirmés dans des études plus importantes et dans des lésions plus variées. Tel est le but de l’étude FUTURE III qui débute et doit randomiser 800 patients (mono- et pluritronculaires) dans le monde (sauf États-Unis) entre le stent ChampionTM et le stent nu ZetaTM. Le stenting direct, les occlusions chroniques, les lésions de bifurcation, les lésions ostiales ne peuvent être inclus. Le critère principal retenu est angiographique et échographique à 4, 6 ou 12 mois (perte de gain et volume de néo-intima). Les premiers résultats sont attendus dès 2005.
Guidant développe parallèlement sa plate-forme VisonTM en cobalt-chrome, un polymère durable, fixé au stent qui contiendra également l’éverolimus et qui sera testé dans l’étude SPRIRIT.
Autres stents issus des pays émergents
À côté de ces deux programmes déjà bien avancés, se développe la mise sur le marché de stents réalisés dans des pays émergents qui pourraient également modifier considérablement l’offre et le coût de ces endoprothèses. Ainsi, le stent Indien InfinniumTM (Sahadjanand Medical Technologies), constitué d’une plate-forme tubulaire recouverte de quatre couches de polymère contenant du paclitaxel (3 mg/mm3) a été testé dans l’étude SIMPLE-1, chez 282 patients (33 % diabétiques, 45 % de pluritronculaires, 46 % de lésions ≥ 19 mm). Les complications cliniques ont été rares (2 décès, 1 IDM) à court terme et 2,5 % seulement de nouvelles revascularisations à 6 mois ont été notées. L’analyse angiographique portant sur 90 patients a montré une perte de gain de 0,2 mm et un taux de resténoses binaires intrastent de 5,9 %, proches des résultats des grandes études déjà citées.
Ces résultats très prometteurs appellent la validation d’une grande étude prospective, lancée en Asie en 2003.
Les autres pistes
À côté de ces programmes cohérents de développement clinique, d’autres pistes sont également explorées. Une liste exhaustive des différents protocoles en cours serait fastidieuse tant le champ d’application est vaste.
La piste anti-inflammatoire est testée à l’aide des stents BiodiVysio dans le cadre d’étude STRIDE avec une certaine efficacité chez les patients en angor instable.
Des stents actifs libérant du 17-bêta-estradiol (BiodiVysio), favorisant la réendothélialisation et limitant la prolifération, ont été utilisés chez les 30 patients de l’étude EASTER. Le contrôle angiographique à 6 mois a montré une resténose chez deux patients (perte de gain 0,54 mm) et l’échographie endocoronaire retrouve un volume de néo-intima de 23,5 %, très supérieur aux chiffres obtenus avec les stents actifs validés.
Et aussi… une amélioration de la réendothélialisation est également ciblée dans une approche originale de stents recouverts de cellules progénitrices des cellules endothéliales (Orbus). Des stents permettant la libération de monoxyde d’azote, molécule clé de l’homéostasie vasculaire (NOBLESSE), des stents recouverts d’oligonucléotides antisens, de vecteurs de transfection virale atténuée...
Au total
Ces voies de recherche fondamentale, bien qu’audacieuses et stimulantes, ne doivent pas faire perdre de vue la réalité clinique bien plus terre à terre. Un stent actif est une alchimie réussie entre une plate-forme acceptable, un revêtement permettant de contrôler plus ou moins bien la libération d’un principe actif agissant sur des voies biologiques menant à la resténose.
Cet équilibre fragile peut parfois réserver de mauvaises surprises comme avec le stent au taxol Quanan associé à des taux de thromboses prohibitifs ou comme avec les stents au batimastat (action antimigration) ne réduisant pas la resténose, ou encore dans le protocole ACTION où les stents actifs à l’actinomycine D (antiprolifération mais non anti-inflammatoire) sont associés à des resténoses intrastent parfois itératives.
Les nouveaux stents actifs demandent une évaluation sérieuse et prolongée dans des populations de taille suffisante avant de pouvoir être recommandés en salle de cathétérisme à côté des stents Cypher™ et Taxus™.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :